题目内容
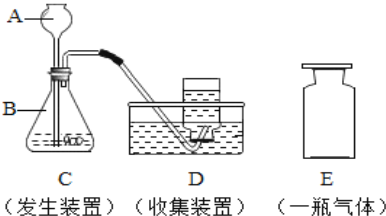
【题目】如图是实验室制取和收集气体的常见装置,回答下列问题:
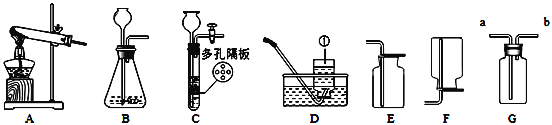
(1)装置D中标号仪器①的名称是_______。
(2)实验室利用C、E组合,可以制取_________气体;写出所制取气体的反应的文字表达式____________________;装置C与装置B相比,有何优点?____________。
(3)在实验室加热高锰酸钾制氧气,反应的符号表达式为____________________,如选用A装置,改进的方法是____________________。用D装置收集氧气,若收集的氧气不纯,可能原因是_________________________、______________________。用排水法开始收集氧气的适宜时刻是______________________________,排水法收集氧气完毕后先移导管后熄灭酒精灯,其原因是_______________。
(4)G装置具有广泛的用途:
①集气:收集某种气体,若需要利用装置G由b端进入,则可推测该气体具有什么性质? ____________________。若用该装置收集氧气,则氧气应从______管进入,验满的方法是_____________________。
②储气:若要将储存在G中的氧气排出,水应从___(填“a”或“b”)口进入。
③量气:若用G装置测量收集到的气体体积,还需要用到的仪器是_______。
【答案】集气瓶二氧化碳;碳酸钙+盐酸→氯化钙+水+二氧化碳;可以随时控制反应的发生和停止,且操作简便KMnO4 ![]() K2MnO4+MnO2+O2;试管口应放一蓬松的棉花团;集气瓶内未装满水;导管口一有气泡就立即收集;气泡连续并均匀地冒出时;防止因试管内压强减小而产生倒吸现象;气体的密度比空气小;a;将带火星的木条放在导管口 b 处,若复燃证明氧气已集满;a;量筒
K2MnO4+MnO2+O2;试管口应放一蓬松的棉花团;集气瓶内未装满水;导管口一有气泡就立即收集;气泡连续并均匀地冒出时;防止因试管内压强减小而产生倒吸现象;气体的密度比空气小;a;将带火星的木条放在导管口 b 处,若复燃证明氧气已集满;a;量筒
【解析】
(1)①是集气瓶。(2)C是固液常温反应制取气体的装置,E是向上排空气法收集气体,CE组合是制取并收集二氧化碳,实验室用石灰石与稀盐酸反应制取二氧化碳,石灰石主要成分是碳酸钙,与稀盐酸反应生成氯化钙、水、二氧化碳。装置C与装置B相比的优点是可以随时控制反应的发生和停止,且操作简便。(3)高锰酸钾在加热条件下发生分解反应生成锰酸钾、二氧化锰、氧气。用高锰酸钾制取氧气,试管口要放一团棉花,以防高锰酸钾堵塞导气管。用排水法收集的氧气不纯,可能原因是集气瓶内未装满水或收集氧气过早。用排水法收集氧气,要当气泡连续并均匀冒出时开始收集。排水法收集氧气完毕后要先移导管后熄灭酒精灯,防止因试管内压强减小水倒吸入试管中而炸裂试管。(4)①若用装置G收集某种气体,气体由b端进入,空气被赶到下方而易从a端排出,所以该气体的密度比空气的密度小。用G装置收集氧气,氧气的密度比空气的密度大,进入以后占据下方空间,空气则被赶到上方空间而易从b端排出,所以氧气应从a管进入,检验该装置内是否收集满氧气的方法是,将带火星的木条放在导管口b处,若复燃证明氧气已集满。②氧气的密度比水小,所以要将储存在G中的氧气排出,水从a口进入,便于氧气排出。③量筒可用来测量液体的体积,所以用G装置测量收集到的气体体积,还需要用到的仪器是量筒。

【题目】元素周期律是学习和研究化学的重要工具。下表是元素周期表的部分信息:
1 H 氢 | 2 He 氦 | |||||||
3 Li 锂 | 4 Be 铍 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 | |
12 Mg 镁 | 13 A1 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | X C1 氯 | 18 Ar 氩 | ||
19 K 钾 | 20 Ca 钙 | …… | ||||||
认真分析信息,回答:
(1)地壳中含量最多的元素的原子序数是_______ ;
(2)分析上表规律,可推知,表中X =________;
(3)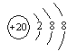 表示的是(写粒子符号)_______;
表示的是(写粒子符号)_______;