题目内容
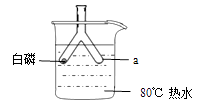
【题目】利用下图装置验证二氧化碳的部分性质,进行如下实验(甲、乙试剂瓶的体积均为250mL)。
实验一:若乙中盛有用紫色石蕊溶液染成的干燥的纸花,关闭K1 , 打开K2 , 通入潮湿的CO2气体,紫色纸花不变色,则甲中所盛试剂可能是。关闭K2 , 打开K1 , 通入潮湿的CO2气体,紫色纸花变红,用化学方程式解释纸花变红的原因。
实验二:若甲中盛有100mLNaOH溶液,乙中盛有100mLCa(OH)2溶液。验证二氧化碳与氢氧化钠发生了反应。
资料:通常状况下,1体积的水约能溶解1体积二氧化碳。
①甲中发生反应的化学方程式为。
②你设计的实验方案是。
【答案】浓硫酸或浓氢氧化钠溶液;CO2 + H2O=H2CO3;CO2+2NaOH=Na2CO3+H2O;关闭K1 , 打开K2 , 往导管中缓缓通入大于250mL的二氧化碳,若乙容器中无浑浊,则说明二氧化碳和氢氧化钠发生了反应
【解析】实验一:若乙中盛有用紫色石蕊溶液染成的干燥的纸花,关闭K1,打开K2,通入潮湿的CO2气体,紫色纸花不变色,则甲中所盛试剂可能是:浓硫酸或浓氢氧化钠溶液;关闭K2,打开K1,通入潮湿的CO2气体,紫色纸花变红,用化学方程式解释纸花变红的原因:CO2+H2O═H2CO3;碳酸能使紫色石蕊试液变红色,所以答案是:浓硫酸或浓氢氧化钠溶液;CO2+H2O═H2CO3
实验二:二氧化碳与氢氧化钠反应生成碳酸钠和水,配平即可;设计的实验方案是:关闭K1,打开K2,往导管中缓缓通入大于250mL的二氧化碳,若乙容器中无浑浊,则说明二氧化碳和氢氧化钠发生了反应;所以答案是:CO2+2NaOH═Na2CO3+H2O;关闭K1,打开K2,往导管中缓缓通入大于250mL的二氧化碳,若乙容器中无浑浊,则说明二氧化碳和氢氧化钠发生了反应.
所以答案是:1、浓硫酸或浓氢氧化钠溶液;2、CO2 + H2O=H2CO3;3、CO2+2NaOH=Na2CO3+H2O;4、关闭K1,打开K2,往导管中缓缓通入大于250mL的二氧化碳,若乙容器中无浑浊,则说明二氧化碳和氢氧化钠发生了反应.
【考点精析】关于本题考查的二氧化碳的化学性质和化学方程式的概念、读法和含义,需要了解化学性质:一般情况下不能燃烧,也不支持燃烧,不能供给呼吸;与水反应生成碳酸;能使澄清的石灰水变浑浊;与灼热的碳反应;遵循原则:①以客观事实为依据 ② 遵守质量守恒定律才能得出正确答案.