题目内容
某学习小组的同学做完木炭还原氧化铜的实验后,观察到固体只有少量为红色,黑色成分含量较多,于是决定对木炭还原氧化铜后的固体成分进行探究.请你参加如下探究过程:
(1)对固体成分猜想.
猜想 I:固体含铜、木炭和氧化铜;
猜想Ⅱ:固体含铜和氧化铜;
猜想Ⅲ:固体含铜和 .
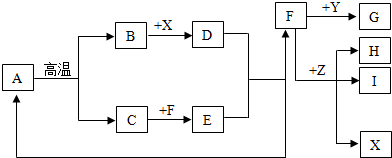
(2)设计实验并进行探究.实验操作流程及现象如图:

该学习小组由上述实验及现象得出固体成分含铜、木炭和氧化铜的结论.你认为此结论 (填“正确”或“不正确”).理由是 .
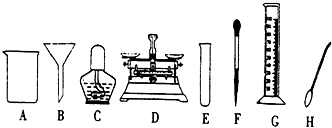
(3)步骤②包括溶解和过滤两步操作,两步操作都用到的仪器有 、 .
(4)写出由固体D生成蓝色溶液E的有关化学方程式: .
(1)对固体成分猜想.
猜想 I:固体含铜、木炭和氧化铜;
猜想Ⅱ:固体含铜和氧化铜;
猜想Ⅲ:固体含铜和
(2)设计实验并进行探究.实验操作流程及现象如图:

该学习小组由上述实验及现象得出固体成分含铜、木炭和氧化铜的结论.你认为此结论
(3)步骤②包括溶解和过滤两步操作,两步操作都用到的仪器有
(4)写出由固体D生成蓝色溶液E的有关化学方程式:
考点:实验探究物质的组成成分以及含量,物质的溶解,过滤的原理、方法及其应用,碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)木炭和氧化铜在加热条件下反应生成铜和二氧化碳,如果木炭和氧化铜都没有完全反应就停止实验,则固体中含有铜、氧化铜和木炭;
如果木炭完全反应,氧化铜过量,则固体中含有铜和氧化铜;
如果氧化铜完全反应,木炭过量,则固体中含有铜和木炭;
(2)氧化铜和稀硫酸反应生成硫酸铜和水,硫酸铜溶液是蓝色溶液;
(3)溶解需要的仪器有烧杯、玻璃棒等;
过滤需要的仪器有烧杯、玻璃棒、漏斗、铁架台等;
(4)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式.
如果木炭完全反应,氧化铜过量,则固体中含有铜和氧化铜;
如果氧化铜完全反应,木炭过量,则固体中含有铜和木炭;
(2)氧化铜和稀硫酸反应生成硫酸铜和水,硫酸铜溶液是蓝色溶液;
(3)溶解需要的仪器有烧杯、玻璃棒等;
过滤需要的仪器有烧杯、玻璃棒、漏斗、铁架台等;
(4)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式.
解答:解:(1)固体中可能含铜、木炭和氧化铜;或含铜和氧化铜;或含铜和木炭.
故填:木炭.
(2)因为溶液A为无色,说明固体中不含氧化铜,所以由上述实验及现象得出固体成分含铜、木炭和氧化铜的结论是不正确的.
故填:不正确;溶液A为无色,说明固体不含氧化铜.
(3)溶解和过滤两步操作都用到的仪器有烧杯和玻璃棒.
故填:烧杯;玻璃棒.
(4)氧化铜和稀硫酸反应的化学方程式为:CuO+H2SO4═CuSO4+H2O.
故填:木炭.
(2)因为溶液A为无色,说明固体中不含氧化铜,所以由上述实验及现象得出固体成分含铜、木炭和氧化铜的结论是不正确的.
故填:不正确;溶液A为无色,说明固体不含氧化铜.
(3)溶解和过滤两步操作都用到的仪器有烧杯和玻璃棒.
故填:烧杯;玻璃棒.
(4)氧化铜和稀硫酸反应的化学方程式为:CuO+H2SO4═CuSO4+H2O.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
下列变化中,属于物理变化的是( )
| A、空气中悬浮颗粒物多时形成雾霾 |
| B、钾原子与氯原子相互作用,变成钾离子和氯离子 |
| C、纸张燃烧 |
| D、碳酸受热分解 |