题目内容
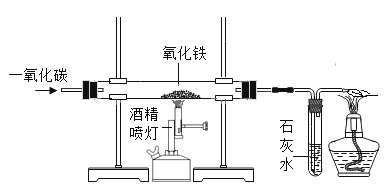
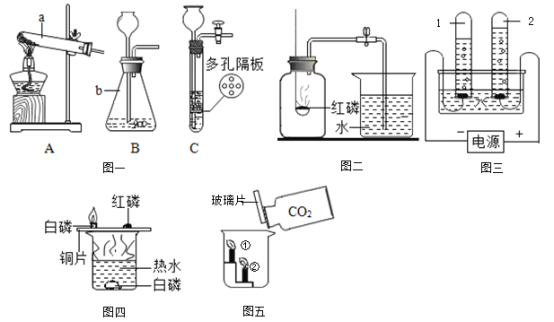
【题目】下图是实验室制取气体的常用装置。
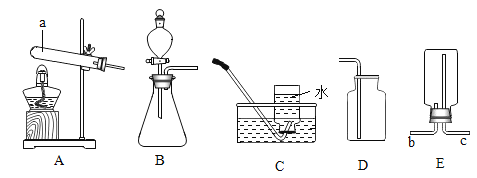
(1)装置中a仪器的名称为____________。
(2)实验室用高锰酸钾制取氧气,应选择的发生装置是________(填装置字母,下同);若要收集较为纯净的氧气,应选择的收集装置是_______:写出该反应的化学方程式_____________。
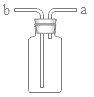
(3)某气体X可以用D装置收集,若改用E装置收集,则气体X从________(填“b”或”“c”)口进。
(4)实验室在常温下用块状固体电石与水反应制取乙炔(C2H2)气体,该反应须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂,你认为上图中最适合制取乙炔的发生装置为__________,工业上常用乙炔作为燃料,其在空气中燃烧生成二氧化碳和水,请写出乙炔燃烧化学方程式___________。
(5)某学习小组用加热氯酸钾和二氧化锰混合物的方法制氧气,反应过程中固体总质量如下图,请计算原混合物中有多少克氯酸钾_________?

【答案】试管 A C ![]() b B
b B 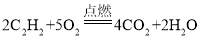 49g
49g
【解析】
(1)考查实验室常见仪器名称,本题涉及到的有酒精灯、试管、铁架台、锥形瓶、分液漏斗、水槽、集气瓶、导管等,仪器a为试管,主要用于加热;
(2)高锰酸钾加热制取氧气是采用固体加热装置,图中A为加热装置,所以选择发生装置为A;收集氧气常采用排水法和向上排空法,由于向上排空法容易有空气混入,所以收集的氧气纯度不如排水法收集的高,所以收集较为纯净的氧气时采用排水法,所以收集装置为C;高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰和氧气,书写化学方程式时注意配平、反应条件及气体符号,所以为![]() ;
;
(3)气体X用D收集,说明气体密度比空气大,当采用E收集时,应从短管b进气,这样气体沉于下部,将上部的空气通过长管a排出,达到收集气体的目的;
(4)根据题目信息可知,乙炔制备是采用固液不加热装置,并且控制水的加入速度,装置B是不需要加热制取气体装置,并且其配置的分液漏斗具有开关,可以控制液体加入的速度;乙炔与氧气在点燃的条件下,生成了二氧化碳和水,书写化学方程式时注意配平、反应条件,所以为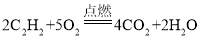 ;
;
(5)氯酸钾在二氧化锰催化作用下分解生成氯化钾和氧气,氧气为气体,被排放到大气中,所以减少的质量则为生成氧气的质量,氧气质量=60g-40.8g=19.2g,设氯酸钾质量为m
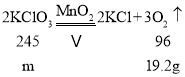
![]() m=49g
m=49g
所以氯酸钾质量为49g。

 阅读快车系列答案
阅读快车系列答案