题目内容
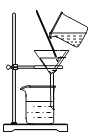
【题目】该图进行的是_____操作,可除去水中_____杂质,此操作中玻璃棒的作用是_____,此操作完成后得到的水是_____(纯净物、混合物),若该水中含有较多钙镁化合物称为_____,用_____能够区分,日常生活中除去水中钙镁化合物的方法是_____若得到净化程度更高的水的方法_____。
【答案】过滤 不溶性固体 引流 混合物 硬水 肥皂水 煮沸 蒸馏
【解析】
据图可以看出,该图进行的是过滤操作,可除去水中不溶性固体杂质;此操作中玻璃棒起到的作用是引流;操作完成后得到的水中仍含有可溶性杂质,故是混合物;若该水中含有较多钙镁化合物称为硬水,用肥皂水能够区分,加入肥皂水后,泡沫多的是软水,泡沫少的是硬水;日常生活中除去水中钙镁化合物的常用方法是煮沸,得到净化程度更高的水的方法是蒸馏。
故填:过滤;不溶性固体;引流;混合物;硬水;肥皂水;煮沸;蒸馏。

【题目】良好的学习习惯和思维方式是学好化学的关键。
(1)请把以下的知识卡片补充完整。
物质 | 类别 | 性质 | 对应的用途 |
①石墨 | 单质 | 质软滑腻 | _____ |
②氦气 | _____ | 通电发有色光 | 制霓虹灯 |
③_____(写俗称) | 氧化物 | 汽化吸热 | 人工降雨 |
(2)“宏观-微观-符号”相结合是化学学科的思维方式。根据下图回答问题:
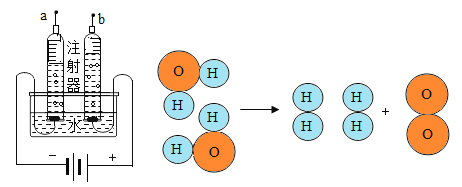
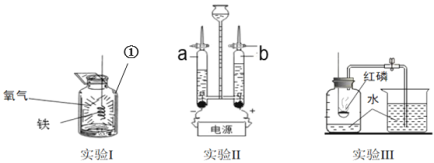
Ⅰ. 宏观现象:点燃a 处气体,产生_____色火焰。
Ⅱ. 微观上述微观示意图所示反应中,没有发生变化的是微粒是氢原子和_____。
Ⅲ. 符号表达:电解水的化学方程式为_____。
【题目】化学课上同学们进行实验验证酸的性质。
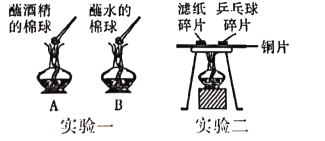
I. 与指示剂作用。

(1)在白色点滴板孔穴1、3中加入紫色石蕊溶液,观察到溶液变_____色。
(2)将无色酚酞溶液滴加到孔穴2、4中,观察到孔穴4中溶液为无色,而孔穴2中溶液变为橙色。同学们猜想孔穴2中的异常现象与硫酸溶液的浓度过高有关,并通过以下实验证明该猜想正确:取少量上述橙色溶液于试管中,加水稀释,观察到的现象是_____。
II. 与铁锈反应。
实验 | 实验试剂 | 实验现象 |
1 | 锈蚀铁钉+10 mL 稀盐酸 | 生成无色气泡,铁锈较快消失,溶液颜色变黄。 |
2 | 锈蚀铁钉+10 mL 稀硫酸 | 生成无色气泡,铁锈减少速度缓慢,溶液颜色未变黄。 |
(提出问题)实验1、2现象不同的原因是什么?
(查阅资料)HCl在水中会解离出H+和Cl-,H2SO4在水中会解离出H+和SO42-。
(假设猜想)可能和溶液中阴离子不同有关。
(进行实验)
实验 | 实验试剂 | 实验现象 |
3 | 锈蚀铁钉+10 mL稀硫酸 + _A_ | 生成无色气泡,铁锈减少速度比实验2快,溶液颜色变黄。 |
4 | 锈蚀铁钉+10 mL稀盐酸 + Na2SO4 | 生成无色气泡,铁锈减少速度比实验1慢,溶液颜色变黄。 |
(解释和结论)
(3)铁锈(主要成分为Fe2O3)和盐酸反应的化学方程式是_____。
(4)实验1中产生的无色气体是_____。
(5)实验3中,物质A是_____。
(6)结合实验1~4,得出的结论是_____。