题目内容
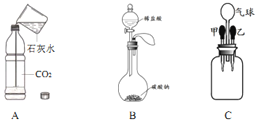
【题目】小强和小明两位同学在实验室用下列装置制取几种气体.

(1)写出图中有标号仪器的名称:a是 ,b是 .
(2)小强想用高锰酸钾制取一瓶氧气应选用的发生装置是 (填装置序号),而小明认为该装置有一个小问题,请你帮助他: ;实验室用该方法制取氧气的化学方程式是 .
(3)在装入药品前,应先进行的一项操作是 .
(4)小明要制取少量CO2,其反应原理是 (用化学方程式表示),他收集该气体的装置是(填装置序号) ,选用该装置的理由是.
(5)为了防止生成的气体从C装置仪器a逸出,必须使a仪器 .
(6)小强和小明还对过氧化氢分解时影响反应速率的部分因素作出探究,并测得相关实验数据.如下表:
实验序号 | H2O2溶液浓度% | H2O2溶液体积/mL | 温度/℃ | MnO2的用量/g | 收集氧气的体积/mL(排水法) | 反应所需时间/s |
① | 5 | 1 | 20 | 0.1 | 2 | 16.75 |
② | 15 | 1 | 20 | 0.1 | 2 | 12.63 |
③ | 20 | 5 | 25 | 0.2 | 4 | 10.70 |
④ | 20 | 5 | 35 | 0.2 | 4 | 8.06 |
从实验③和④对比可知,化学反应速率与 有关.通过实验①与②对比可知,化学反应速率与反应物的有关.若用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,加适量水稀释,产生氧气的总质量 .(选填“减小”或“不变”或“增大”).
【答案】(1)长颈漏斗、水槽;
(2)A、在试管口塞一团棉花、2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)检查装置气密性;
(4)CaCO3+2HCl=CaCl2+CO2↑+H2O、D;
(5)下端管口伸入液面以下;
(6)温度、不变.
【解析】(1)a是长颈漏斗,通过长颈漏斗可以向反应容器中注入液体药品;b是水槽,常用于排水法收集气体;
(2)用高锰酸钾制取氧气需要加热,应该用A装置作为发生装置;为了防止高锰酸钾进入导管,应该在试管口塞一团棉花;高锰酸钾受热分解的化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)为了防止装置漏气影响实验,在装入药品前,应先检查装置的气密性;
(4)碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;二氧化碳能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用D装置收集;
(5)为了防止生成的气体从仪器a中逸出,必须使a仪器的末端浸没在液体中;
(6)从表中分析可知:③④是温度不同其他条件相同,明显是对温度影响化学反应速度的探究;①②是过氧化氢浓度不同而其他的反应时各种量均相同,可知这一过程是考查反应物的浓度与反应速度的关系;从表中分析可知:①②是过氧化氢浓度不同而其他的反应时各种量均相同,可知这一过程是考查反应物的浓度与反应速度的关系,且反应物的浓度越大,化学反应速率越快,所以用一定量的质量分数为15%的过氧化氢溶液制氧气,在不影响产生氧气质量的前提下,为了减慢反应速率,可采取加水稀释过氧化氢溶液的措施,故加适量水稀释,产生氧气的总质量不变.

 教学练新同步练习系列答案
教学练新同步练习系列答案