题目内容
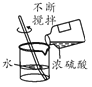
【题目】今天又是化学实验室开放日,老师拿出两瓶无标签的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体。我们对此气体展开了一系列探究:
①此气体是什么物质?验证它的实验方案如下:
猜想 | 实验步骤 | 现象及结论 |
此气体可能是:_____ | _____ | _____ |
②产生此气体的化学方程式可能是_____。
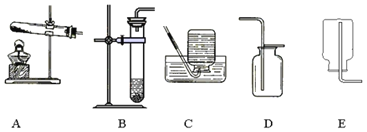
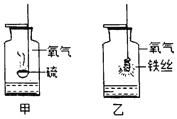
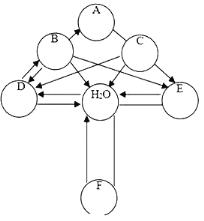
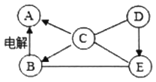
③我想制取该气体,采用的发生装置可选取如图中的_____(填序号),收集装置是_____。
【答案】O2 将带火星的木条深入集气瓶中 木条复燃,该气体为氧气(合理即可) ![]() B D
B D
【解析】
①如果用双氧水和二氧化锰制氧气就不需要加热,氧气的检验方法是:将带火星的木条伸入集气瓶中,木条复燃,证明是氧气;
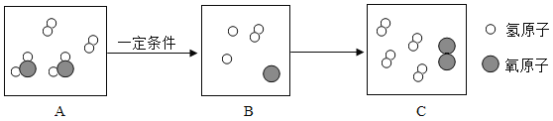
②过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,化学方程式为:![]() ;
;
③实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,因此不需要加热。二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集。

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案【题目】探究影响过氧化氢分解速率的影响因素。
(査阅资料)常温下,H2O2较稳定不易分解;CuSO4溶液、FeCl3溶液和红砖粉末等都能作为H2O2分解制取O2的催化剂。
(分析交流)写出实验室用H2O2溶液和MnO2制取O2的化学方程式:_____。
(实验设计)取相同体积的过氧化氢溶液分别进行下列实验。
实验编号 | 温度/℃ | 催化剂 | 过氧化氢浓度/% |
① | 20 | 无 | 2 |
② | 20 | 无 | 5 |
③ | 20 | 5滴FeCl3溶液 | 5 |
④ | 20 | 5滴CuSO4溶液 | 5 |
(1)实验①②探究的是_____。要探究CuSO4溶液能否做H2O2分解的催化剂,应选择的实验编号是_____。
(2)要定性比较两种催化剂的催化效果,可通过观察_____来实现。要定量比较两者的催化效果,可测量生成等体积气体所需的_____。
(3)同学们实验时还观察到,在H2O2溶液内滴入FeCl3溶液,溶液逐渐由黄色变为浅绿色,最终变回浅黄色。查阅资料得知:FeCl3溶液一般呈黄色,FeCl2溶液一般呈浅绿色。由此你对催化剂有何新的认识?_____。