题目内容
【题目】用“侯氏制碱法”制得的纯碱中常含有少量的氯化钠.为测定某纯碱样品中碳酸钠的质量分数,小雯同学称取该样品5.6 g加入到盛有100g稀盐酸的烧杯中,完全反应后称得烧杯中的溶液质量为103.4g.(反应的化学方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O)
求:
(1)完全反应后生成二氧化碳的质量为g.
(2)该纯碱样品中碳酸钠的质量分数.(结果精确到0.1%)
【答案】
(1)2.2
(2)解:设碳酸钠的质量为X
Na2CO3+2HCl=2NaCl+ | CO2↑+H2O |
106 | 44 |
X | 2.2g |
![]() 解得:X=5.3g
解得:X=5.3g
该纯碱样品中碳酸钠的质量分数为:
![]() ×100%=94.6%
×100%=94.6%
【解析】解:(1)由质量生守定律及题意可知,生成的二氧化碳的质量为:5.6 g+100g﹣103.4g=2.2g;
【考点精析】解答此题的关键在于理解根据化学反应方程式的计算的相关知识,掌握各物质间质量比=系数×相对分子质量之比.

【题目】钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将125g盐酸分成5等份,逐次加到用50片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题. 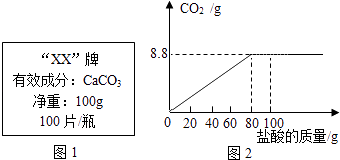
第1次 | 第3次 | 第4次 | |
加入盐酸的质量(g) | 25 | 25 | 25 |
剩余固体的质量(g) | 45 | a | 30 |
(1)该品牌补钙药剂中CaCO3的质量分数是 , a的数值为
(2)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数).
(3)求恰好完全反应时所得溶液的溶质质量分数(写出计算过程,计算结果保留一位小数).
【题目】对下列实验指定容器中的液体,其解释没有体现液体的主要作用的是( )
A | B | C | D | |
实验装置 |
|
|
|
|
解释 | 集气瓶中水:吸收放出的热量 | 量筒中的水:通过水体积的变化得出O2体积 | 集气瓶中的水:冷却溅落融熔 | 集气瓶中的水:先将集气瓶内的空气排尽,后便于观察O2何时收集满 |
A.A
B.B
C.C
D.D
【题目】实验与探究是化学学习的重要方法和内容.
(1)第一小组的同学制取了三瓶干燥的氧气,将足量燃着的硫和木炭分别伸入其中的两个集气瓶中使其充分燃烧,硫燃烧的化学方程为;
(2)实验结束后,实验台上仍有三瓶气体(如图),老师请第二小组同学鉴别这三瓶气体,探究报告如下列,请你补充完整.
操作步骤 | 现象 | 结论 |
1、分别 | B瓶 | B瓶是二氧化硫 |
2、向剩余两瓶气体中分别 倒入少量澄清的石灰 水,振荡. | A瓶 | A瓶是 |
(3)评价与反思:
①二小组第1步实验操作应特别注意,不要;
②第二小组同学提出第一小组实验前应在B瓶中放少量水,其目的是