题目内容
【题目】在电解水实验中,若b试管连接正极得到10毫升气体,则a 试管得到毫升气体,极生成的气体能使带火星的木条复燃。极生成的气体能燃烧,呈火焰。该实验说明水是由和组成。此反应的的化学方程式为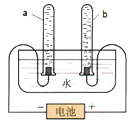
【答案】20;正;负;淡蓝色火焰;氢元素;氧元素;2H2O ![]() 2H2↑+ O2↑
2H2↑+ O2↑
【解析】电解水的口诀记忆:正氧负氢,氢二氧一;即正极产生氧气,负极产生氢气,产生的氢气与氧气的体积比为2:1。所以电解水时,正极产生10mL氧气,同时负极产生20mL氢气;负极生成的氢气能够燃烧,淡蓝色火焰;据质量守恒定律可知反应前后元素种类不变,通过电解水生成氢气和氧气,可得出水是一种化合物(氧化物),水是由氢元素和氧元素组成的,反应的的化学方程式为 2H2O ![]() 2H2↑+ O2↑。
2H2↑+ O2↑。
【考点精析】认真审题,首先需要了解电解水实验(电解水的实验:A.装置―――水电解器B.电源种类---直流电C.加入硫酸或氢氧化钠的目的----增强水的导电性D.化学反应:2H2O=== 2H2↑+ O2↑),还要掌握水的构成(水是由氢、氧元素组成的;一个水分子是由2个氢原子和1个氧原子构成的;化学变化中,分子可分而原子不可分)的相关知识才是答题的关键.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目