题目内容
【题目】元素周期表是学习和研究化学的重要工具。下图是元素周期表的一部分。
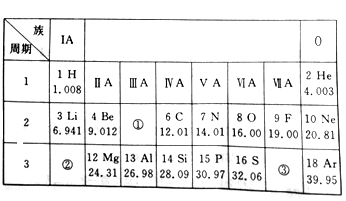
(1)很多科学家对元素周期期表的发现和完善做出了重大贡献,请写出其中一位科学家的名字:_________。
(2)学习化学后,我们学会了从微观角度认识事物。
根据下列四种粒子的结构示意图,回答问题。
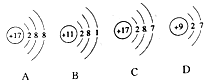
①它们属于同种元素的是______(填序号,下同)。
②图C是某元素的原子结构示意图,该元素在元素周期表中的位置是______(选填①或②或③)。
(3)原子序数为12的元素的原子在化学反应中易_______(填“得”或“失”),形成离子符号是_______。该元素在化合物中的化合价为_____价,该元素和原子序数为9的元素组成的化合物是________(填化学式)。
(4)探究金属钠与水反应时,发现有气体生成,收集气体并点燃,有明显爆鸣声,向反应后溶液中滴加酚酞试剂,溶液呈红色。由此推断,钠与水反应的化学方程式为_________;由以上信息,你对物质的结构与性质之间的关系有什么认识__________。
【答案】(1)门捷列夫或张青莲(1分)
(2)①AC(1分) ② ③(1分)
(3)失(1分或失2个) Mg2+(1分)+2(1分) MgF2(1分)
(4)2Na+2H2O=2NaOH+H2↑(2分)结构决定性质,性质反映结构(1分)
【解析】(1)张青莲为铕元素的相对原子质量的测定做出了卓越的贡献,、门捷列夫在化学学科中的主要成就,是发现了元素周期律,并首次编制了元素周期表,(2)①在原子结构示意图中,小圆圈表示原子核,圆圈内的数字表示质子数,质子数决定原子的类别,弧线表示电子层,最外层电子数决定原子的化学性质;(3)当最外层电子数小于4时,反应中易失去电子成为阳离子;当最外层电子数大于4时,反应中易得到电子成为阴离子;原子核外只有一个电子层且电子数为2,或者最外层电子数为8的结构为稳定结构,不易得失电子。离子符号书写:元素(或根)符号右上角的数字表示一个离子带电荷的数值,数字在左,正负号在右,电荷数为1时,1不写; Mg2+;一个原子失去电子数等于正价的数值;+2;化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉约减,得化学式右下角的数字,数字为1时不写; MgF2;(4)金属钠与水反应时,发现有气体生成,收集气体并点燃,有明显爆鸣声,说明生成氢气;向反应后溶液中滴加酚酞试剂,溶液呈红色,说明生成氢氧化钠。由此推断,钠与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑。由以上信息可知,原子的结构决定性质,性质反映结构。