题目内容
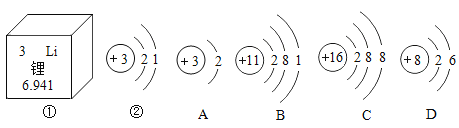
【题目】小明同学依据描述书写的化学符号:①两个氮分子:2N2;②由三个氧原子构成的臭氧分子:3O;③粒子结构示意图 表示的粒子:S;④两个铁离子:2Fe3+;⑤2MnO42-:表示2个锰酸根离子;⑥+2价的镁元素:Mg2+;⑦H2S中的“2”表示2个氢原子。其中正确的有( )
表示的粒子:S;④两个铁离子:2Fe3+;⑤2MnO42-:表示2个锰酸根离子;⑥+2价的镁元素:Mg2+;⑦H2S中的“2”表示2个氢原子。其中正确的有( )
A.①③④B.①④⑤C.①③④⑤D.①④⑤⑦
【答案】B
【解析】
①分子前面的数字表示分子个数,两个氮分子:2N2,故正确;
②由三个氧原子构成的臭氧分子:O3,故错误;
③粒子结构示意图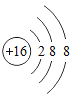 表示硫原子得2个电子变为硫离子:S2-,故错误;
表示硫原子得2个电子变为硫离子:S2-,故错误;
④离子符号前面的数字表示离子个数,两个铁离子:2Fe3+,故正确;
⑤离子符号前面的十字表示离子个数2MnO42-:表示2个锰酸根离子,故正确;
⑥+2价的镁元素:![]() ,故错误;
,故错误;
⑦H2S中的“2”表示1个硫化氢分子中含有2个氢原子,故错误;
所以正确的有:①④⑤;故选:B。

【题目】氨气是无色、密度比空气小、极易溶于水![]() 的刺激性气体,强烈刺激眼睛和黏膜。可用于制造化肥、制冷剂,亦可用于炸药、染料、塑料和一些药物的生产等。请回答下列问题:
的刺激性气体,强烈刺激眼睛和黏膜。可用于制造化肥、制冷剂,亦可用于炸药、染料、塑料和一些药物的生产等。请回答下列问题:
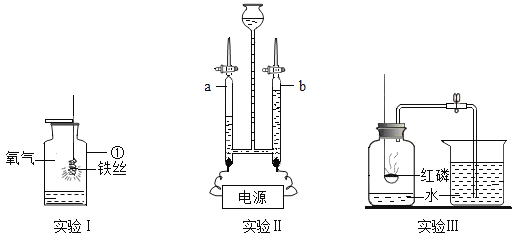
(一)氨气的合成是人类科学技术的重大突破,工业上合成氨的微观示意图如下。
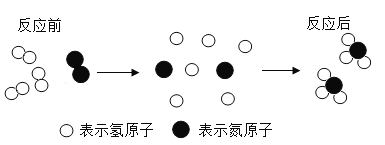
(1)该化学变化过程中不可再分的微粒符号为____________________________。
(2)该反应条件是高温、高压及催化剂,则化学方程式为_________________。
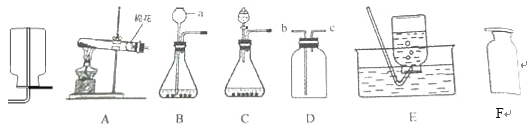
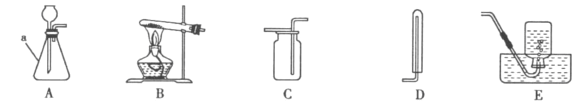
(二)在实验室里,我们可选用下图中所提供的实验装置制取氨气并进行相关实验探究。
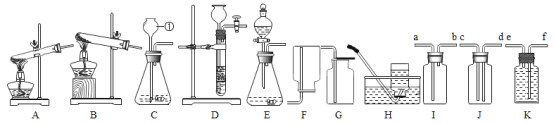
(3)写出标号仪器①的名称___________________________________.
(4)实验室制备氨气是利用氯化铵和熟石灰固体加热来生成,发生反应的化学方程式为____________,选用的装置代码为____________________.其验满的方法是_____________________________________.
(三)天天兴趣小组的同学决定通过实验设计定量研究氨气中氮、氢两种元素的质量比。
(查阅资料)
I.![]()
II. ![]() ;
;![]()
III.干燥剂种类:氯化钙、浓硫酸、氢氧化钠、碱石灰、无水硫酸铜等
(方案设计)天天小组同学将产生氨气装置依据设计流程连接成实验探究装置如下图所示。
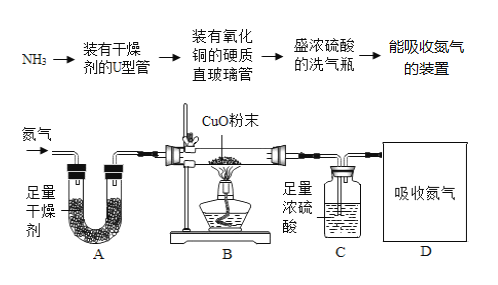
(实验观察)
(5)可作A中U形管内干燥剂的物质是________________________________.
(6)在B装置直玻璃管内出现的现象是____________________________________.
(7)通常把金属氧化物失去氧转化为金属的过程,称为金属氧化物的还原。那么B装置中玻璃管内发生后的还原过程是指_______________________________________________.
(数据分析)待充分反应后,测得A、B、C、D四个装置前后的质量变化如下表所示:
装置编号 | A | B | C | D |
记录数据 | 增加0.1g | 减少4.8g | 增加6.0g | 增加2.8g |
(8)可选择与计算需要数据相应的装置编号为________________________.
(9)通过计算:氮元素质量______________,氢元素质量__________________.列比例式计算氮、氢元素的质量比为____________________________.