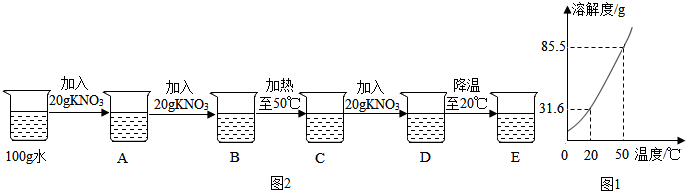
题目内容
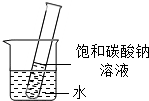 碳酸钠的溶解度随着温度升高而增大20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某种物质后,试管中有晶体析出.
碳酸钠的溶解度随着温度升高而增大20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某种物质后,试管中有晶体析出.(1)若加入能溶于水的物质使碳酸钠晶体析出,可加入什么物质?
(2)若加入能与水反应的物质使碳酸钠晶体析出,可加入什么物质?写出有关的化学方程式
考点:晶体和结晶的概念与现象,溶解时的吸热或放热现象
专题:溶液、浊液与溶解度
分析:(1)根据要使碳酸钠晶体析出需要降低温度,其中硝酸铵溶于水吸热进行解答;
(2)根据干冰溶于水吸热,二氧化碳和水反应生成碳酸进行解答.
(2)根据干冰溶于水吸热,二氧化碳和水反应生成碳酸进行解答.
解答:解:(1)要使碳酸钠晶体析出需要降低温度,其中硝酸铵溶于水吸热,温度降低;故填:硝酸铵;
(2)干冰溶于水吸热,温度降低,也能使碳酸钠晶体析出,二氧化碳和水反应生成碳酸,化学方程式为CO2+H2O═H2CO3.故填:干冰;CO2+H2O═H2CO3.
(2)干冰溶于水吸热,温度降低,也能使碳酸钠晶体析出,二氧化碳和水反应生成碳酸,化学方程式为CO2+H2O═H2CO3.故填:干冰;CO2+H2O═H2CO3.
点评:通过回答本题知道了物质溶于水吸热和放热情况,属于基础知识的考查.

练习册系列答案
相关题目
抗甲型H1N1流感的有效药物达菲(Tamiflu),可用从香料八角中提取的莽草酸(C7H10O5)来制得,下列有关莽草酸的说法中正确的是( )
| A、莽草酸中含有5个氧原子 |
| B、莽草酸分子由碳、氢、氧三种元素组成 |
| C、莽草酸水溶液的PH<7 |
| D、莽草酸中各元素的质量比为7:10:5 |
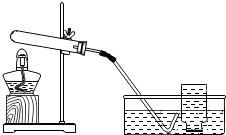
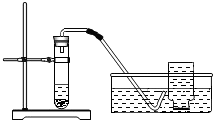
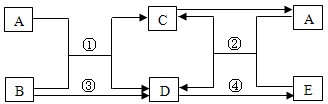
 双氧水常用于消毒、漂白等方面,它是含过氧化氢(H2O2)的溶液,含H2O230%的水溶液以二氧化锰做催化剂时,可迅速分解放出氧气,现欲制取干燥纯净的氧气,可采用如图装置.
双氧水常用于消毒、漂白等方面,它是含过氧化氢(H2O2)的溶液,含H2O230%的水溶液以二氧化锰做催化剂时,可迅速分解放出氧气,现欲制取干燥纯净的氧气,可采用如图装置.