题目内容
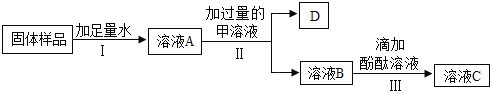
【题目】祺祺在实验室发现了一瓶标签残缺的无色溶液(如图甲所示),为确认其中的溶质,她设计并进行了如下探究活动,请回答下列问题。
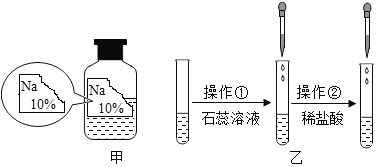
[猜想与假设]其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
[资料查阅]上述四种物质的相关信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
[探究过程]
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是_____;在进行操作②时有无色无味的气体产生,由此又可排除假设物质中的_____。
[探究结论]祺祺由此推断出该溶液中的溶质可能是上述假设物质中的_____。
[探究反思]实验结束后,祺祺将上述实验中所有的物质都倒入盛有“实验室制取二氧化碳”实验中所得废液的废液缸中,观察到有气泡产生,最终逐渐产生了少量白色沉淀。请帮祺祺同学写出产生气泡的反应的化学方程式:_____;最终废液缸中一定存在的溶质除石蕊外还有_____。
【答案】溶液变成蓝色 氢氧化钠 Na2CO3 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 氯化钠(或NaCl)
【解析】
探究过程:
NaCl、NaOH、Na2CO3和NaHCO3中只有氯化钠溶液为中性,而其余的溶液都显碱性,若溶质不是NaCl,滴加石蕊试液会变成蓝色;在进行操作2滴加稀盐酸时有无色无味的气体产生,说明不是氢氧化钠,因为氢氧化钠和盐酸反应无明显现象;
探究结论:
根据计算可以知道,在20℃时饱和碳酸氢钠的质量分数=![]() ,题目中标注的溶液的质量分数为10%,所以这瓶试剂不可能的是碳酸氢钠溶液,而碳酸钠溶液的溶质质量分数可以等于10%,因此可能是Na2CO3;
,题目中标注的溶液的质量分数为10%,所以这瓶试剂不可能的是碳酸氢钠溶液,而碳酸钠溶液的溶质质量分数可以等于10%,因此可能是Na2CO3;
探究反思:
盛有“实验室制取二氧化碳”实验中所得废液的废液缸中一定含有氯化钙,可能存在盐酸。由上述分析可知,溶液中含有碳酸钠,则碳酸钠和盐酸反应会产生二氧化碳气体,反应的化学方程式是:Na2CO3+2HCl=2NaCl+H2O+CO2↑,与稀盐酸反应完后,碳酸钠与氯化钙反应生成了碳酸钙沉淀和氯化钠,所以,最终废液缸中一定存在的溶质除石蕊外还NaCl。

 阅读快车系列答案
阅读快车系列答案【题目】冬季雾霾频发。某校社会实践小组的同学们,对某地区雾霾的成分、成因、危害及防治产生了浓厚的兴趣并开启了项目性学习之旅。
[信息检索]雾是浮游在空中的大量微小水滴。霾是可吸入颗粒物浓度较高造成的能见度较低的现象。霾的主要成分肯含有可溶性硫酸盐、硝酸盐、铵盐、不溶性有机物、黑碳、金属元素和其它元素。
[提出问题]探究霾中是否含有黑碳
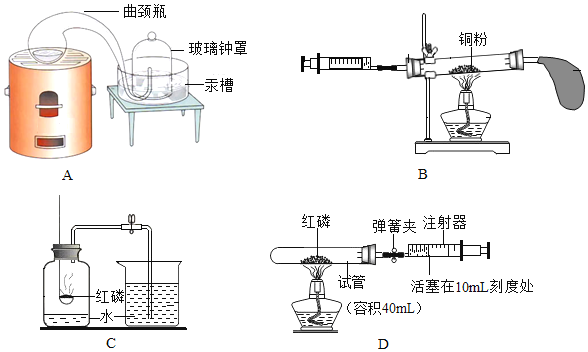
活动:同学们设计了如图所示的创新实验。( 图中残渣为霾的样品)
[实验步骤]①滴入过氧化氢溶液制取O2,排出装置内空气后,再在导管口接上气球。
②向右边的凹槽内滴入澄清的石灰水。
③接通电源,用用热电阻丝点燃残渣。
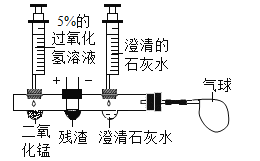
[实验现象]残渣剧烈燃烧,澄清石灰水浑浊,气球变大。
上述现象中澄清石灰水变浑浊的方程式是____,针对上述活动你得到的结论是_____,理由是_________。
[交流研讨][能力发展]请你联系实际填写关于雾霾的问卷调查表:
项目 | 雾霾频发的成因 | 控制雾霾频发的做法 | 政府采取的应急措施 |
① | 能源结构不同 | 推广太阳能发电 | 人工降雨 |
② | 烧散煤取暖 | _________ | 向空中或地面洒水 |
③ | _____________ | 推广新能源汽车 | 私家车限号出行 |
【题目】在学习实验室制取二氧化碳选用试剂研究中,一般都会以块状大理石和稀盐酸、粉末状大理石与稀盐酸、碳酸钠与稀盐酸、块状大理石与稀硫酸进行对比实验探究。化 学兴趣小组就除反应物状态以外影响大理石与稀盐酸反应快慢因素进行了如下探究。
(提出问题)大理石与稀盐酸反应的快慢还会受哪些因素的影响?
(猜想假设)
假设一:可能与温度的高低有关。 假设二:可能与稀盐酸的浓度有关。
(设计并实验)小组成员用不同质量分数的稀盐酸和不同环境温度下进行如下实验:
实验 序号 | 盐酸的质量分数 (均取 20mL) | 大理石 的质量 | 实验环 境温度 | 收集相同体积的二氧 化碳所用时间(秒) |
1 | 10% | 2g | 20℃ | 59.8 |
2 | 10% | 2g | 35℃ | 41.7 |
3 | 20% | 2g | 20℃ | 35.5 |
4 | 20% | 2g | 35℃ | 27.2 |
(1) 写出实验室制取二氧化碳的反应化学方程式_____。
(收集证据)
(2) 要比较不同温度对反应快慢的影响应选择实验编号是_____;要比较不同质量分 数的稀盐酸对反应快慢的影响应选择实验编号是_____。
(总结反思)
(3)小组经过讨论分析得出如下结论:
a、温度与大理石与稀盐酸反应快慢的关系:_____;
b、稀盐酸浓度与大理石与稀盐酸反应快慢的关系:___________________。
(4)本实验除用收集相同体积气体所需要的时间这一产生产物的快慢来定量比较反应速率快慢外,还可以采用其他什么方法来比较反应速率的快慢(除观察产生气泡的快慢)? 答:_____。