题目内容
以下A、B、C都是研究物质组成的实验.从研究方法得知,
A实验是利用可燃物消耗瓶内的________,使瓶内压强减小来推测空气里氧气含量的.
B实验是通过证明生成物的________来推断水的组成的.
而C实验与________(填实验代号)实验的方法相同.

氧气 元素种类 B
分析:通过测定空气里氧气含量的实验、电解水实验、甲烷燃烧实验的原理可以得出本题的答案.
解答:测定空气里氧气含量的实验原理是:红磷燃烧,消耗集气瓶中的氧气,从而使集气瓶内外产生压强差,烧杯中的水在压强差的作用下流入集气瓶中,继而测定出流入集气瓶中水的体积,再用水的体积与集气瓶的容积相比,就能得到实验的结论.
电解水实验的原理是:水通电分解成两种气体,通过实验现象确定两种气体是氢气和氧气,根据质量守恒定律可知水中含有氢、氧两种元素;通过气体的密度和体积,可以计算出两种气体的质量比,根据质量守恒定律可知,该质量比就是水中氢、氧元素的质量比,通过该质量比可以得到水的组成和构成.
甲烷燃烧的现象是:发出蓝色火焰,放热,烧杯壁上有水珠出现,生成使澄清石灰水变浑浊的气体.由“烧杯壁上有水珠出现”说明生成了水,水由氢、氧元素组成,根据质量守恒定律可知甲烷中一定含有氢元素;由“生成使澄清石灰水变浑浊的气体”说明生成了二氧化碳,二氧化碳有碳、氧元素组成,根据质量守恒定律可知甲烷中一定含有碳元素;通过实验测定出水和二氧化碳的质量后,还可以确定甲烷中是否含有氧元素.
通过上述分析可以知道A实验是利用可燃物消耗瓶内的氧气,使瓶内压强减小来推测空气里氧气含量的;B实验是通过证明生成物的元素种类(或“组成”或“成分”)来推断水的组成的;而C实验与B实验的方法相同.
故答案为:(1)氧气;(2)元素种类(或“组成”或“成分”);(3)B.
点评:本题主要考查测定空气里氧气含量的实验、电解水实验、甲烷燃烧实验的原理,难度稍大.
分析:通过测定空气里氧气含量的实验、电解水实验、甲烷燃烧实验的原理可以得出本题的答案.
解答:测定空气里氧气含量的实验原理是:红磷燃烧,消耗集气瓶中的氧气,从而使集气瓶内外产生压强差,烧杯中的水在压强差的作用下流入集气瓶中,继而测定出流入集气瓶中水的体积,再用水的体积与集气瓶的容积相比,就能得到实验的结论.
电解水实验的原理是:水通电分解成两种气体,通过实验现象确定两种气体是氢气和氧气,根据质量守恒定律可知水中含有氢、氧两种元素;通过气体的密度和体积,可以计算出两种气体的质量比,根据质量守恒定律可知,该质量比就是水中氢、氧元素的质量比,通过该质量比可以得到水的组成和构成.
甲烷燃烧的现象是:发出蓝色火焰,放热,烧杯壁上有水珠出现,生成使澄清石灰水变浑浊的气体.由“烧杯壁上有水珠出现”说明生成了水,水由氢、氧元素组成,根据质量守恒定律可知甲烷中一定含有氢元素;由“生成使澄清石灰水变浑浊的气体”说明生成了二氧化碳,二氧化碳有碳、氧元素组成,根据质量守恒定律可知甲烷中一定含有碳元素;通过实验测定出水和二氧化碳的质量后,还可以确定甲烷中是否含有氧元素.
通过上述分析可以知道A实验是利用可燃物消耗瓶内的氧气,使瓶内压强减小来推测空气里氧气含量的;B实验是通过证明生成物的元素种类(或“组成”或“成分”)来推断水的组成的;而C实验与B实验的方法相同.
故答案为:(1)氧气;(2)元素种类(或“组成”或“成分”);(3)B.
点评:本题主要考查测定空气里氧气含量的实验、电解水实验、甲烷燃烧实验的原理,难度稍大.

练习册系列答案
相关题目
请你参与某校学习小组进行的以下研究性学习的过程,并协助完成相关任务.
【研究课题】探究热水壶底部水垢的主要成分
【查阅资料】该小组同学通过查阅资料知道:
①天然水中一般都含有Ca2+、Mg2+、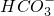 等离子.
等离子.
②在加热条件下,这些离子趋于生成溶解度更小的物质,即水垢.(主要成分为碳酸盐、碱等物质的混合物).
③碱石灰的化学成分是CaO与NaOH的混合物,可吸收水分和酸性气体(如二氧化碳).
④有关物质的溶解性如下:
| 物质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(OH)2 | Mg(OH)2 | CaCO3 | MgCO3 |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 微溶 |
【设计方案】(1)甲同学在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,取上层清液加入______,没有白色沉淀产生,说明水垢中无Ca(OH)2.
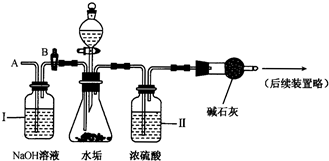
(2)乙同学设计了下列实验装置,进一步确定水垢中是否含有碳酸盐的成分.其主要实验步骤如下:
①按下图组装仪器,检查装置气密性,再将50g水垢试样放入锥形瓶中,并加入足量某酸溶液;
②测量一定时间内干燥管内物质增加的质量;
③待锥形瓶中不再产生气泡时,打开活塞B,从导管A处缓缓放入一定量的空气;
④再次称量干燥管内物质增加的质量;
⑤重复③和④的操作,直至干燥管内物质质量不变,并称得干燥管质量增加了24g.

讨论:
a.步骤①所加的酸溶液是______.
b.从导管A处缓缓鼓入一定量的空气时,装置Ⅰ的作用是______.
c.研究性学习小组的同学通过简单计算,认为水垢中一定含有MgCO3,理由是______.
【实验结论】通过上述探究可知:水垢的主要成分有______.
请你参与某校学习小组进行的以下研究性学习的过程,并协助完成相关任务.
【研究课题】探究热水壶底部水垢的主要成分
【查阅资料】该小组同学通过查阅资料知道:
①天然水中一般都含有Ca2+、Mg2+、 等离子.
等离子.
②在加热条件下,这些离子趋于生成溶解度更小的物质,即水垢.(主要成分为碳酸盐、碱等物质的混合物).
③碱石灰的化学成分是CaO与NaOH的混合物,可吸收水分和酸性气体(如二氧化碳).
④有关物质的溶解性如下:
【提出猜想】水垢的主要成分一定含有Mg(OH)2和______,可能含有Ca(OH)2和______.
【设计方案】(1)甲同学在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,取上层清液加入______,没有白色沉淀产生,说明水垢中无Ca(OH)2.
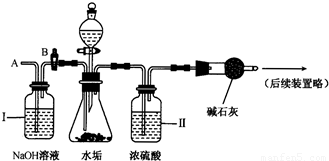
(2)乙同学设计了下列实验装置,进一步确定水垢中是否含有碳酸盐的成分.其主要实验步骤如下:
①按下图组装仪器,检查装置气密性,再将50g水垢试样放入锥形瓶中,并加入足量某酸溶液;
②测量一定时间内干燥管内物质增加的质量;
③待锥形瓶中不再产生气泡时,打开活塞B,从导管A处缓缓放入一定量的空气;
④再次称量干燥管内物质增加的质量;
⑤重复③和④的操作,直至干燥管内物质质量不变,并称得干燥管质量增加了24g.
讨论:
a.步骤①所加的酸溶液是______.
b.从导管A处缓缓鼓入一定量的空气时,装置Ⅰ的作用是______.
c.研究性学习小组的同学通过简单计算,认为水垢中一定含有MgCO3,理由是______.
【实验结论】通过上述探究可知:水垢的主要成分有______.
【研究课题】探究热水壶底部水垢的主要成分
【查阅资料】该小组同学通过查阅资料知道:
①天然水中一般都含有Ca2+、Mg2+、
 等离子.
等离子.②在加热条件下,这些离子趋于生成溶解度更小的物质,即水垢.(主要成分为碳酸盐、碱等物质的混合物).
③碱石灰的化学成分是CaO与NaOH的混合物,可吸收水分和酸性气体(如二氧化碳).
④有关物质的溶解性如下:
| 物质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(OH)2 | Mg(OH)2 | CaCO3 | MgCO3 |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 微溶 |
【设计方案】(1)甲同学在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,取上层清液加入______,没有白色沉淀产生,说明水垢中无Ca(OH)2.
(2)乙同学设计了下列实验装置,进一步确定水垢中是否含有碳酸盐的成分.其主要实验步骤如下:
①按下图组装仪器,检查装置气密性,再将50g水垢试样放入锥形瓶中,并加入足量某酸溶液;
②测量一定时间内干燥管内物质增加的质量;
③待锥形瓶中不再产生气泡时,打开活塞B,从导管A处缓缓放入一定量的空气;
④再次称量干燥管内物质增加的质量;
⑤重复③和④的操作,直至干燥管内物质质量不变,并称得干燥管质量增加了24g.

讨论:
a.步骤①所加的酸溶液是______.
b.从导管A处缓缓鼓入一定量的空气时,装置Ⅰ的作用是______.
c.研究性学习小组的同学通过简单计算,认为水垢中一定含有MgCO3,理由是______.
【实验结论】通过上述探究可知:水垢的主要成分有______.