题目内容
【题目】某化学小组用熟石灰配制石灰水时,发现装满熟石灰的塑料试剂瓶已经破埙.
提出向题1 试剂是否变质?
猜想 ①没有变质,成分是氢氧化钙 ②全部变质,成分是碳酸钙
③部分变质,成分是氢氧化钙和碳酸钙
进行实验1
步骤 | 操 作 | 现 象 | 结论 |
1 | 取样品于试管中,加水,滴入2~3滴酚酞试液 | ____________________________________________ | 猜想③正确 |
2 | 向试管中继续 加入过量的___________ | ____________________________________________ |
提出问题2 如何测定试剂中碳酸钙的质量分数?
进行实验2 小丽同学设计了如图所示装置进行碳酸钙的质量分数测定:
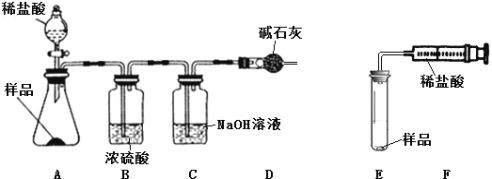
取一定质量的样品放入锥形瓶中,加入过量稀盐酸(不考虑稀盐酸的挥发),测量装置C在反应前后的总质量,即可计算出试剂中碳酸钙的质量分数。请写出稀盐酸与碳酸钙发生反应的化学方程式 ____________________________________________
说明:装置气密性良好,操作无误,各步反应完全。
反思与评价
(1)小文同学认为小丽得到的结果有较大的误差,理由是_________________________________
(2)小文同学用图E、F所示装置(注射器活塞的摩擦力很小,忽略不计)完成测量。注
射器除了贮存、加注稀盐酸外,还有的作用是____________________________________________
交流与讨论 实验结束后将A、C、E中废液倒入一个干净的废液缸中,观察到有沉淀生成。
(1)同学们将废液过滤并讨论滤液中溶质的成分,该滤液中一定存在的溶质是______________________
(2)经实验确认废液成分,处理后绿色排放
【答案】进行实验1
步骤 | 操 作 | 现 象 | 结论 |
1 | 取样品于试管中,加水,滴入2~3滴酚酞试液 | 无色酚酞变红色 | 猜想③正确 |
2 | 向试管中继续加入过量的 稀盐酸 | 有气泡冒出 |
进行实验2 CaCO3+2HCl=CaCl2+H2O+CO2↑
反思与评价(1)生成的二氧化碳有一部分停留在AB中,没有被C吸收(2)测量体积
交流与讨论氯化钠
【解析】
试题分析:猜想③正确,说明其中含有氢氧化钙和碳酸钙,因此操作是取样品于试管中,加水,滴入2~3滴酚酞试液,如果变红,说明其中含有氢氧化钙,向试管中继续加入过量的稀盐酸,如果产生气泡说明含有碳酸钙固体,稀盐酸与碳酸钙发生反应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑;小文同学认为小丽得到的结果有较大的误差,理由是生成的二氧化碳有一部分停留在AB中,没有被C吸收,小文同学用图E、F所示装置(注射器活塞的摩擦力很小,忽略不计)完成测量。注射器除了贮存、加注稀盐酸外,还有的作用是测量体积,实验结束后将A、C、E中废液倒入一个干净的废液缸中,观察到有沉淀生成。将废液过滤并讨论滤液中溶质的成分,该滤液中一定存在的溶质是氯化钠。

 科学实验活动册系列答案
科学实验活动册系列答案