题目内容
化学老师张××指导某化学兴趣学习小组进行了一个有趣的实验探究:测定鸡
蛋壳的主要成分碳酸钙的质量分数.实验如下:将鸡蛋壳洗净、干燥并捣碎后,称取8.0g放在烧杯里,然后往烧杯中加入足量的稀盐酸50mL(密度1.1g/ml),充分反应后,称得反应剩余物为59.92g(假设其他物质不与盐酸反应).请回答:
(1)上述稀盐酸的质量为________g,产生二氧气体的质量为________g.
(2)计算该鸡蛋壳中碳酸钙的质量分数. (要求写出计算过程)
(3)该稀盐酸中HCI的质量分数应不小于多少?(要求写出计算过程)
解:
盐酸的质量为:50mL×密度1.1g/ml=55g
产生二氧气体的质量为:8.0g+55g-59.92g=3.08g
设:碳酸钙的质量为X,氯化氢的质量为Y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
x y 3.08g
 =
=
 =
=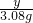
x=7g
y=5.11g
 ×100%=87.5%
×100%=87.5%
 ×100%=9.3%
×100%=9.3%
答:(1)55g 3.08g
(2)计算该鸡蛋壳中碳酸钙的质量分数为87.5%
(3)该稀盐酸中HCl的质量分数应不小于9.3%
分析:根据密度公式的变形质量=体积×密度求出盐酸的质量50mL×密度1.1g/ml=55g,由题意分析得出产生二氧气体的质量为8.0g+55g-59.92g=3.08g,再根据方程式中二氧化碳的质量求出碳酸钙和氢化氢的质量,进一步求出鸡蛋壳中碳酸钙的质量分数和该稀盐酸中HCI的质量分数应不小于多少.
点评:此题是溶质的质量分数与化学方程式的综合计算,首先要正确写出方程式,再根据题意仔细分析各量关系,认真计算,方可求解.
盐酸的质量为:50mL×密度1.1g/ml=55g
产生二氧气体的质量为:8.0g+55g-59.92g=3.08g
设:碳酸钙的质量为X,氯化氢的质量为Y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
x y 3.08g
 =
=
 =
=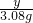
x=7g
y=5.11g
 ×100%=87.5%
×100%=87.5% ×100%=9.3%
×100%=9.3%答:(1)55g 3.08g
(2)计算该鸡蛋壳中碳酸钙的质量分数为87.5%
(3)该稀盐酸中HCl的质量分数应不小于9.3%
分析:根据密度公式的变形质量=体积×密度求出盐酸的质量50mL×密度1.1g/ml=55g,由题意分析得出产生二氧气体的质量为8.0g+55g-59.92g=3.08g,再根据方程式中二氧化碳的质量求出碳酸钙和氢化氢的质量,进一步求出鸡蛋壳中碳酸钙的质量分数和该稀盐酸中HCI的质量分数应不小于多少.
点评:此题是溶质的质量分数与化学方程式的综合计算,首先要正确写出方程式,再根据题意仔细分析各量关系,认真计算,方可求解.

练习册系列答案
相关题目