题目内容
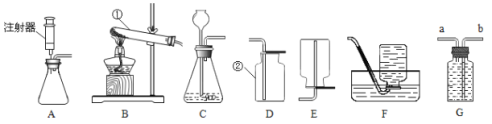
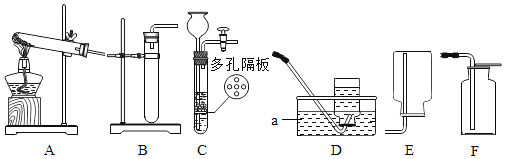
【题目】请结合图1回答问题:
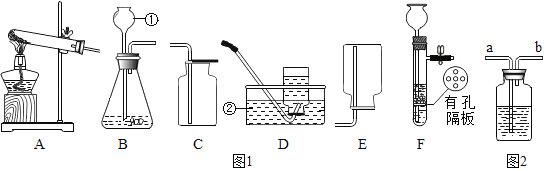
(1)写出有标号的仪器名称:①________,②________。
(2)实验室用高锰酸钾制取O2的化学式表达式为________________________________,用A、D装置制取O2时,为防止高锰酸钾进入导管,采取的措施是___________。实验结束时先_________________防止水倒流。使用该组合制取O2的另一种方法的化学式表达式为_________________。
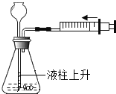
(3)实验室用B、C装置制取CO2的化学式表达式为________________,若将发生装置由B改为F,其优点是____________________。
(4)某兴趣小组将新制得的CO2通入澄清的石灰水中,未见浑浊。分析原因可能有下列两种情况:
①可能是错用了较浓的盐酸,CO2中混入了较多的氯化氢气体,为验证此想法甲同学查阅资料知:氯化氢气体的水溶液能使紫色石蕊试液变红,于是将气体通入紫色石蕊试液。你认为此方案 ________(填“是”或“否”)可行。
②可能是生成的CaCO3又与CO2反应生成了可溶性的Ca(HCO3)2,反应的化学式表达式为________。
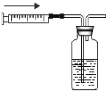
(5)实验室用锌粒和稀盐酸制氢气,选择的发生装置是___________。用图2装置收集氢气时,瓶内先装满水,气体从 ____________ (填“a”或“b”)处导管通入。
【答案】长颈漏斗 水槽 KMnO4![]() K2MnO4+MnO2+O2 试管口放棉花团 将导管移出水面 KClO3
K2MnO4+MnO2+O2 试管口放棉花团 将导管移出水面 KClO3![]() KCl+O2 CaCO3+HCl
KCl+O2 CaCO3+HCl![]() CaCl2+H2O+CO2 控制反应的发生和停止(随开随停) 否 CaCO3+H2O+CO2
CaCl2+H2O+CO2 控制反应的发生和停止(随开随停) 否 CaCO3+H2O+CO2![]() Ca(HCO3)2 B b
Ca(HCO3)2 B b
【解析】
(1)长颈漏斗方便加液体药品,水槽是盛水的仪器,故答案为:①长颈漏斗; ②水槽;
(2)如果用高锰酸钾或氯酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,化学式表达式为:![]() ;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,化学式表达式为:
;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,化学式表达式为:![]() ;
;
(3)实验室制取二氧化碳,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,化学式表达式为:![]() ;F装置的优点是:能控制反应的发生和停止;;
;F装置的优点是:能控制反应的发生和停止;;
(4)①可能是错用了较浓的盐酸,二氧化碳中混入了较多的氯化氢气体,为验证此想法甲同学的方案不可行,因为二氧化碳和水生成碳酸,碳酸使紫色变红色;
②可能是生成的![]() 又与
又与![]() 和水反应生成了可溶性的
和水反应生成了可溶性的![]() ;
;
(5)实验室用锌粒和稀盐酸制氢气,为固液反应不需加热型,选择的发生装置是B,用图2装置收集氢气时,瓶内先装满水,气体从短管b处进入,因为氢气的密度比水小。

 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案【题目】空气中氧气含量测定的再认识。
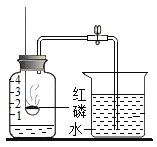
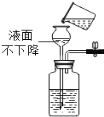
请回忆教材用红磷燃烧来粗略测定空气中氧气含量的装置。
(1)实验时,取下橡胶塞,点燃红磷迅速伸入集气瓶中,这时看到的现象是___________;红磷燃烧时红磷燃烧的反应符号表达式_____________,属________反应(填“化合”或“分解”)。
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内__________减小,烧杯中水倒吸到集气瓶。但是实验结果液面往往偏低,其可能原因是________。
(问题提出)有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧, 因此通过上述实验,测置结果与理论值误差较大。
(实验改进)
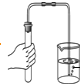
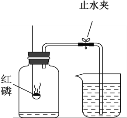
Ⅰ.根据铁在空气中生锈的原理设计下图实验装置,再次测定空气中氧气含量。装置中饱和食盐水、活性炭会加速铁生锈。
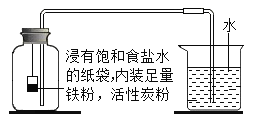
Ⅱ.测得实验数据如下表
测量项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
体积/mL | 80.0 | 54.5 | 126.0 |
(交流表达)
(1)铁生锈过程发生复杂的化学反应(一个缓慢氧化的过程),最终生成铁锈。根据表中的数据计算,改进实验后测得空气中氧气体积分数是________(计算结果精确到0.1 %) 。
(2)从实验原理角度分析,改进后的实验结果比前者准确度更高的原因是:________。
【题目】以下是某研究小组探究影响反应速率部分因素的相关实验数据。(注:在制取气体的实验中,常用收集相同体积的气体所用时间来判断反应速率的快慢,所用时间越短反应的速率就越快。)
实验序号 | H2O2溶 液浓度% | H2O2溶液体积/mL | 温度℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
③ | 30 | 5 | 35 | 2 | 49.21 | |
④ | 30 | 5 | 55 | 2 | 10.76 |
(1)写出该反应的文字表达式:____;
(2)通过实验①和②对比可知,化学反应速率与____有关;从实验____和____对比可知,化学反应速率与温度的关系是:____。
(3)此反应中二氧化锰的作用是:____。
(4)在实验中,该小组同学发现,二氧化锰颗粒大小可能会影响反应速率,请设计实验方案进行验证:_____。