题目内容
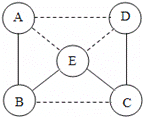
【题目】下图是一些微粒的结构示意图和硒元素的相关信息,回答下列问题:
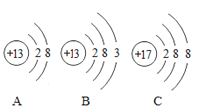
(1)A、B、C中属于阳离子的是__________,其离子符号为____________。
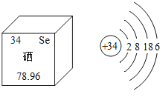
(2)硒与元素周期表中第二周期的______(填元素名称)化学性质相似,写出硒元素和钠元素组成化合物的化学式_____________。
【答案】A Al3+ 氧 Na2Se
【解析】
(1)微粒A的质子数大于核外电子数,属于阳离子,微粒B的质子数等于电子数,属于原子,微粒C的质子数小于电子数,属于阴离子,故填A;
A微粒为铝离子,其符号为Al3+,故填Al3+。
(2)由图可知,硒原子的最外层电子数为6,与元素周期表中第二周期的氧元素的原子最外层电子数相同,故填氧;
硒元素的化合价为-2价,钠元素的化合价为+1价,两种元素组成化合物的化学式为Na2Se,故填Na2Se。

【题目】在老师的指导下,小华和小明利用如图1所示装置对氯酸钾制氧气进行了深入的探究学习。
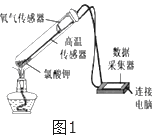
资料:
①氯酸钾的熔点约为356℃,二氧化锰的分解温度约为535℃。用酒精灯给物质加热,受热物质的温度一般约为400℃左右;
②不同配比是指氯酸钾和二氧化锰混合物中,氯酸钾和二氧化锰的质量比;
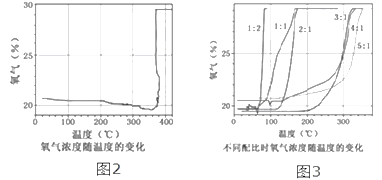
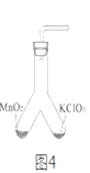
③氯酸钾分解时,传感器得到氧气浓度随温度的变化示意图(图2)及不同配比时氧气浓度随温度的变化示意图(图3)如下:
请回答问题:
(1)二氧化锰在535℃以上分解生成四氧化三锰和氧气,其反应方程式为_____________。
(2)分析图2,氧气的浓度随温度升高逐渐减小,在380℃突然增大的原因是氯酸钾分解温度______(填“高于”、“等于”或“低于”)其熔点。
(3)分析图3,氯酸钾分解温度随物质配比变化的规律是_____________。
(4)为证实二氧化锰的催化作用,小华利用如图4装置进行如表所示的实验:
步骤 | 实验操作 | 实验现象 |
I | 检查气密性 | |
II | 分别在“Y”形管两侧支管中加入少量的二氧化锰和氯酸钾塞紧橡皮塞 | |
III | 分别用酒精灯先后加热二氧化锰和氯酸钾,用带火星木条放在导气管口。 | 加热左侧支管,可观察到 加热右侧支管,可观察到 |
IV | 冷却后,将“Y”形管左侧支管中部分二氧化锰混入右侧支管中,振荡“Y”形管,加热,用带火星木条放在导管口。 | 加热时间短于步骤III,木条很快复燃。 |
请回答:
①完善步骤Ⅲ中的填空:加热左侧支管,可观察到_______,加热左侧试管的目的是_______。加热右侧支管,可观察到_______
②步骤Ⅳ中,将二氧化锰混入右侧支管有余热的氯酸钾中的操作方法是_________。
③小华认为根据步骤Ⅳ的实验现象就能说明二氧化锰是氯酸钾分解的催化剂,但小明不同意她的观点,小明认为还需证明在此反应中二氧化锰的__________和__________不变。后来在老师的指导下,小华完善了实验方案,最终验证了自己的结论,则氯酸钾制取氧气的化学方程式为__________。