题目内容
(2011?天水)天然水受到污染后,净化时需要时需要运用科学方法.请回答:
①天然水污染的来源有
②常用的净水方法有
③漂白粉可用于水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(Cl0)2],次氯酸钙可发生如下反应
Ca(Cl0)2+H2O+x═CaCO3↓+2HClO,则x的化学式为
①天然水污染的来源有
工业三废的任意排放
工业三废的任意排放
(写出一种即可).②常用的净水方法有
过滤
过滤
(写出一种即可).③漂白粉可用于水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(Cl0)2],次氯酸钙可发生如下反应
Ca(Cl0)2+H2O+x═CaCO3↓+2HClO,则x的化学式为
CO2
CO2
.分析:①根据水的污染源主要有:未经处理而排放的工业废水;未经处理而排放的生活污水;大量使用化肥、农药、除草剂的农田污水;堆放在河边的工业废弃物和生活垃圾;水土流失;矿山污水进行解答;
②根据常用的净水方法有:沉淀、过滤出水中杂质,蒸馏、煮沸,除去硬水中的钙镁离子;吸附除去水中异味进行解答;
③根据化学反应前后原子的种类和数目不变进行解答.
②根据常用的净水方法有:沉淀、过滤出水中杂质,蒸馏、煮沸,除去硬水中的钙镁离子;吸附除去水中异味进行解答;
③根据化学反应前后原子的种类和数目不变进行解答.
解答:解:①造成水污染的原因主要有:工业三废的任意排放,农药化肥的大量使用,生活污水的随意排放;
故填:工业三废的任意排放;
②净水就是除去水中的杂质,常用的方法有沉降、过滤、吸附、消毒、蒸馏等;
故填:过滤;
③根据化学反应前后原子的种类和数目不变和Ca(Cl0)2+H2O+x═CaCO3↓+2HClO可知1个x中含有1个碳原子和2个氧原子,是二氧化碳.
故填:CO2.
故填:工业三废的任意排放;
②净水就是除去水中的杂质,常用的方法有沉降、过滤、吸附、消毒、蒸馏等;
故填:过滤;
③根据化学反应前后原子的种类和数目不变和Ca(Cl0)2+H2O+x═CaCO3↓+2HClO可知1个x中含有1个碳原子和2个氧原子,是二氧化碳.
故填:CO2.
点评:本题主要考查学生对水污染的来源的认识和水的净化方法的掌握.

练习册系列答案
相关题目

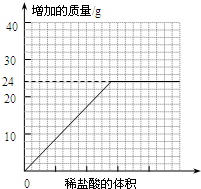
 相对分子质量小者放出的气体多.分析曲线图可知:水垢中一定含有
相对分子质量小者放出的气体多.分析曲线图可知:水垢中一定含有