题目内容
甲、乙两位同学在学完酸的化学性质后,做了如下实验:

实验结束,甲先将废液缓慢倒入一洁净的废液缸中;随后乙也将废液倒入到同一废液缸中.
【观察与分析】同学观察到废液缸中先有气泡产生,然后又出现了白色沉淀.
产生的气体是 ;
产生的白色沉淀CaCO3是Na2CO3溶液与 溶液反应产生的.
【提出问题】最终废液中含有什么溶质?
【猜测与假设】猜想一:废液中含有NaCl、CaCl2两种物质.
猜想二:废液中含有NaCl、Na2CO3两种物质.
【实验设计与探究】
【反思与评价】
(1)【猜想与假设】不完整,请补充:猜想三:
(2)甲同学的【实验设计与探究】实际上是不合理的,不合理的理由是: .

实验结束,甲先将废液缓慢倒入一洁净的废液缸中;随后乙也将废液倒入到同一废液缸中.
【观察与分析】同学观察到废液缸中先有气泡产生,然后又出现了白色沉淀.
产生的气体是
产生的白色沉淀CaCO3是Na2CO3溶液与
【提出问题】最终废液中含有什么溶质?
【猜测与假设】猜想一:废液中含有NaCl、CaCl2两种物质.
猜想二:废液中含有NaCl、Na2CO3两种物质.
【实验设计与探究】
| 实验方案 | 实验现象 | 结论 | |
| 甲 | 取少量废液于试管中,向其中滴加Na2CO3溶液 | 无明显现象 | 猜想一不成立 猜想二成立 |
| 乙 | 取少量废液于试管中,向其中滴加CaCl2溶液 | 出现白色沉淀 | 猜想一不成立 猜想二成立 |
(1)【猜想与假设】不完整,请补充:猜想三:
(2)甲同学的【实验设计与探究】实际上是不合理的,不合理的理由是:
考点:实验探究物质的组成成分以及含量,酸的化学性质,盐的化学性质
专题:科学探究
分析:【观察与分析】废液缸中先有气泡产生,然后又出现了白色沉淀,说明液体中有酸和碳酸根及钙离子;所以知甲同学的试管含有CaCl2、HCl;乙同学的试管中含有NaCl、Na2CO3所以产生的气体是二氧化碳,生成的沉淀是碳酸钠与氯化钙反应产生的;
【反思与评价】(1)甲、乙同学的废液混合之后,发生的反应是Na2CO3+2HCl═2NaCl+H2O+CO2↑和CaCl2+Na2CO3═CaCO3↓+2NaCl,由“废液缸中后又出现了白色沉淀”可知废液缸中存在CaCO3,则最后废液中的溶质不可能还有HCl,废液中的溶质有以下三种可能:①NaCl和 CaCl2;②NaCl和Na2CO3; ③NaCl;
(2)甲的探究方案具有不确定性;
【反思与评价】(1)甲、乙同学的废液混合之后,发生的反应是Na2CO3+2HCl═2NaCl+H2O+CO2↑和CaCl2+Na2CO3═CaCO3↓+2NaCl,由“废液缸中后又出现了白色沉淀”可知废液缸中存在CaCO3,则最后废液中的溶质不可能还有HCl,废液中的溶质有以下三种可能:①NaCl和 CaCl2;②NaCl和Na2CO3; ③NaCl;
(2)甲的探究方案具有不确定性;
解答:解:【观察与分析】废液缸中先有气泡产生,然后又出现了白色沉淀,通过反应可知:①盐酸和氢氧化钙溶液生成氯化钙和水,②盐酸和碳酸钠生成氯化钠和水和二氧化碳;另外还应考虑盐酸和碳酸钠过量;所以知甲同学的试管含有CaCl2、HCl;乙同学的试管中含有NaCl、Na2CO3;故产生的气体为盐酸和碳酸钠反应产生的二氧化碳气体,沉淀是由剩余的碳酸钠和氯化钙反应生成;
【反思与评价】(1)猜想一是两混合液充分反应后,氯化钙剩余;猜想二是碳酸钠剩余,猜想三则是二者恰好完全反应,只有氯化钠;
(2)甲同学向废液加入碳酸钠溶液无明显现象,废液中的溶质可能是猜想二,也可能是猜想三,故不合理;
股答案为:【观察与分析】二氧化碳;氯化钙;
【反思与评价】NaCl;如果废液中只含有氯化钠,滴加碳酸钠溶液也是无明显现象
【反思与评价】(1)猜想一是两混合液充分反应后,氯化钙剩余;猜想二是碳酸钠剩余,猜想三则是二者恰好完全反应,只有氯化钠;
(2)甲同学向废液加入碳酸钠溶液无明显现象,废液中的溶质可能是猜想二,也可能是猜想三,故不合理;
股答案为:【观察与分析】二氧化碳;氯化钙;
【反思与评价】NaCl;如果废液中只含有氯化钠,滴加碳酸钠溶液也是无明显现象
点评:本题主要考查化学实验方案的设计与评价,根据物质的性质和物质间的反应规律,学会运用猜想与事实验证的方法和技巧处理实验问题.解答此题的关键是只需要对所涉及的各个反应中反应物是否恰好完全反应做出假设,若反应物恰好完全反应,则废液中的溶质只有生成物,若反应结束后反应物仍有剩余,则废液中的溶质除了生成物外还有剩余的反应物.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
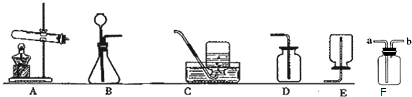
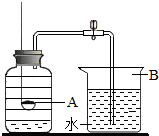 空气中氧气含量的测定.回答下列问题:
空气中氧气含量的测定.回答下列问题: