题目内容
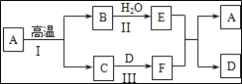
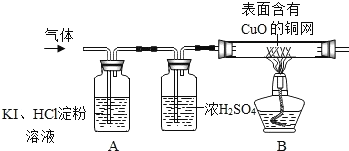
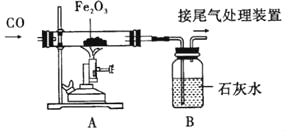
【题目】某兴趣小组利用如图装置研究一氧化碳和氧化铁的反应。
已知:①碳和氧化铁反应时,也会生成少量四氧化三铁、氧化亚铁等固体物质。
②铁、四氧化三铁都具有磁性;氧化亚铁不具有磁性。
③四氧化三铁、氧化亚铁均能和稀盐酸反应化学方程式分别为:Fe3O4+8HCl=2FeCl3+FeCl2+4H2O;
FeO+2HCl=FeCl2+H2O。
回答下列问题:
(1)硬质玻璃管中发生的主要反应的化学方程式为_____。
(2)停止加热前_____(填“需要”或“不需要”)先断开A和B的连接来防止石灰水倒吸,理由是_____。
(3)如何处理尾气:_____,处理的原因:_____。
(4)反应后硬质玻璃管及剩余固体总质量会_____(选填“增加”或“减少”)。
(5)两同学分别设计了甲、乙两个方案验证生成的黑色固体是否都是铁:
甲方案:用磁铁实验观察固体是否全部被吸引。
乙方案:取一定量固体加入足量稀盐酸,有气泡产生,观察固体是否全部消失。
丙同学认为以上实验方案均不正确,甲方案不正确的原因是_____;乙方案不正确的原因是_____。
为进一步完善乙方案以达到实验目的需要对乙方案进行改进,请设计实验方案。_____。
【答案】3CO+Fe2O3![]() 2Fe+3CO2 不需要 反应结束后还需要继续通入一氧化碳直到装置冷却,所以不会发生倒吸 在B导管口处加一个燃着的酒精灯 一氧化碳有毒,污染环境 减少 四氧化三铁也能被磁铁吸引 四氧化三铁和氧化亚铁也能溶解于稀盐酸 测定产生氢气的体积或质量,根据测得的数据计算出铁的质量是否等于固体质量
2Fe+3CO2 不需要 反应结束后还需要继续通入一氧化碳直到装置冷却,所以不会发生倒吸 在B导管口处加一个燃着的酒精灯 一氧化碳有毒,污染环境 减少 四氧化三铁也能被磁铁吸引 四氧化三铁和氧化亚铁也能溶解于稀盐酸 测定产生氢气的体积或质量,根据测得的数据计算出铁的质量是否等于固体质量
【解析】
(1)硬质玻璃管中发生的主要反应是在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳;故填:3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
(2)停止加热前 不需要先断开A和B的连接来防止石灰水倒吸,原因是反应结束后还需要继续通入一氧化碳直到装置冷却,所以不会发生倒吸;故填:不需要;反应结束后还需要继续通入一氧化碳直到装置冷却,所以不会发生倒吸;
(3)一氧化碳有毒,属于空气污染物,所以要进行尾气处理,由于一氧化碳具有可燃性,所以可以在B导管口处加一个燃着的酒精灯,故填:在B导管口处加一个燃着的酒精灯;一氧化碳有毒,污染环境;
(4)硬质玻璃管内发生的主要反应是3CO+Fe2O3![]() 2Fe+3CO2,反应前的固体是氧化铁,反应后的固体是铁,所以反应后硬质玻璃管及剩余固体总质量会减少;故填:减少;
2Fe+3CO2,反应前的固体是氧化铁,反应后的固体是铁,所以反应后硬质玻璃管及剩余固体总质量会减少;故填:减少;
(5)因为四氧化三铁也能被磁铁吸引,所以甲方案不正确;因为四氧化三铁和氧化亚铁也能溶解于稀盐酸,所以乙方案也不正确;铁与盐酸反应生成氢气,而四氧化三铁和氧化亚铁与盐酸反应不会生成氢气,所以可对实验方案作如下改进:测定产生氢气的体积或质量,根据测得的数据计算出铁的质量是否等于固体质量;故填:四氧化三铁也能被磁铁吸引;四氧化三铁和氧化亚铁也能溶解于稀盐酸;测定产生氢气的体积或质量,根据测得的数据计算出铁的质量是否等于固体质量。

 目标测试系列答案
目标测试系列答案