题目内容
学习了MnO2对过氧化氢有催化作用的知识后,小敏同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了如下探究.
【猜想】Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后 .
【实验】用天平称量0.2gCuO,取5ml、5%的过氧化氢溶液于试管中,进行如图实验:

(1)填写表格:
(2)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、 .
(3)除催化剂外,影响化学反应速率的因素还有哪些?如表是小敏同学实验探究的相关数据.
A.通过实验对比可知,化学反应速率与反应物浓度、 有关.
B.化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子的概率有关.试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是: .
【猜想】Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后
【实验】用天平称量0.2gCuO,取5ml、5%的过氧化氢溶液于试管中,进行如图实验:

(1)填写表格:
| 步骤①现象 | 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 带火星的小木条不复燃 | 溶液中有气泡放出, | 猜想Ⅰ、Ⅱ不成立,猜想Ⅲ成立 |
(3)除催化剂外,影响化学反应速率的因素还有哪些?如表是小敏同学实验探究的相关数据.
| 实验 序号 | H2O2溶 液浓度/% | H2O2溶液体积/mL | 温度/℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | 0 | 2 | 49.21 |
| ④ | 30 | 5 | 55 | 0 | 2 | 10.76 |
B.化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子的概率有关.试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是:
考点:催化剂的特点与催化作用,影响化学反应速率的因素探究,过滤的原理、方法及其应用,氧气的检验和验满
专题:科学探究
分析:Ⅲ、根据催化剂的定义回答.
(1)根据氧化铜对过氧化氢的分解有催化作用回答③现象;根据催化剂的定义和特点回答⑥结果;根据催化剂的定义和特点回答⑦现象.
(2)根据过滤的操作过程回答,要注意仪器与材料或用品不同;
(3)A.①②是过氧化氢浓度不同而其他条件相同,这种设计是验证反应物浓度对反应速度的影响;③④则是温度不同其他条件相同,是对温度影响化学反应速度的探究;
B.反应物越浓在溶液中离子的密度会更大,离子间结合的机会更多,分析时应从微观离子着手.
(1)根据氧化铜对过氧化氢的分解有催化作用回答③现象;根据催化剂的定义和特点回答⑥结果;根据催化剂的定义和特点回答⑦现象.
(2)根据过滤的操作过程回答,要注意仪器与材料或用品不同;
(3)A.①②是过氧化氢浓度不同而其他条件相同,这种设计是验证反应物浓度对反应速度的影响;③④则是温度不同其他条件相同,是对温度影响化学反应速度的探究;
B.反应物越浓在溶液中离子的密度会更大,离子间结合的机会更多,分析时应从微观离子着手.
解答:解:Ⅲ、催化剂的特点是“一变,两不变”,即反应速率变,质量和化学性质不变.
(1)氧化铜对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故现象是有气泡,带火星的木条复燃;催化剂的特点是“一变,两不变”,反应前后其质量不变,所以氧化铜的质量仍为0.2g;催化剂的特点是“一变,两不变”,其中反应速率改变,这里是加快,所以现象是溶液中有气泡放出,带火星的木条复燃.
(2)过滤用到的仪器有:铁架台(带铁圈)、漏斗、滤纸、烧杯、玻璃棒;
(3)A.从表中分析可知:①②是过氧化氢浓度不同而其他的反应时各种量均相同,可知这一过程是考查反应物的浓度与反应速度的关系;则是温度不同其他条件相同,是对温度影响化学反应速度的探究,且温度越高,过氧化氢分解速率越大;
B.反应物浓度大时溶液中的离子数量较多,反应的接触面较大反应速度自然变快.
故答案为::Ⅲ、质量和化学性质不变;
(1)填表:
(2)玻璃棒;滤纸;
(3)A.温度;
B.反应物浓度越大,单位体积的反应物中含有的粒子数越多,粒子间碰撞的概率越大,化学反应速率越快.
(1)氧化铜对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故现象是有气泡,带火星的木条复燃;催化剂的特点是“一变,两不变”,反应前后其质量不变,所以氧化铜的质量仍为0.2g;催化剂的特点是“一变,两不变”,其中反应速率改变,这里是加快,所以现象是溶液中有气泡放出,带火星的木条复燃.
(2)过滤用到的仪器有:铁架台(带铁圈)、漏斗、滤纸、烧杯、玻璃棒;
(3)A.从表中分析可知:①②是过氧化氢浓度不同而其他的反应时各种量均相同,可知这一过程是考查反应物的浓度与反应速度的关系;则是温度不同其他条件相同,是对温度影响化学反应速度的探究,且温度越高,过氧化氢分解速率越大;
B.反应物浓度大时溶液中的离子数量较多,反应的接触面较大反应速度自然变快.
故答案为::Ⅲ、质量和化学性质不变;
(1)填表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 剧烈反应,产生大量气泡 | 固体质量为0.2g | 带火星木条复燃 |
(3)A.温度;
B.反应物浓度越大,单位体积的反应物中含有的粒子数越多,粒子间碰撞的概率越大,化学反应速率越快.
点评:催化剂、催化作用是初中重要基本概念之一,是考查的重点和热点,主要考查对催化剂、催化作用概念的理解,对催化效率影响因素的探究等.

练习册系列答案
相关题目
钢铁是全世界应用最多的金属材料.下列关于钢铁及制品的说法错误的是( )
| A、铁合金有生铁和钢两种,其性能比纯铁更优良 | ||||
B、高炉中炼铁的主要反应可表示为:3C+2Fe2O3
| ||||
| C、配制含硫酸铜的波尔多液时不能用铁制容器盛装 | ||||
| D、家用菜刀经洗净擦干后可防止生锈 |
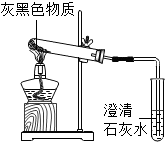 镁是一种银白色的金属,但实验室看到的镁条常常有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?甲同学认为可能是MgO:乙同学认为可能是Mg2(OH)2CO3;丙同学认为可能是Mg(OH)2.
镁是一种银白色的金属,但实验室看到的镁条常常有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?甲同学认为可能是MgO:乙同学认为可能是Mg2(OH)2CO3;丙同学认为可能是Mg(OH)2.