题目内容
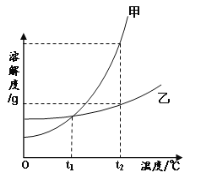
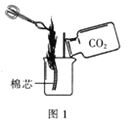
【题目】(1)某学习小组收集到一些铜绿(碱式碳酸铜)他们拟通过化学反应获得铜,根据下图资料,回答下列问题。

①碱式碳酸铜的物理性质之一是 。
②用稀硫酸、铁为原料将碱式碳酸铜转化为铜,反应的化学方程式是: 。
(2)另一小组收集了一些硫酸铁与硫酸亚铁的混合物,如果经实验测知,硫酸铁与硫酸亚铁混合物中含硫a﹪,则其中含铁的质量分数为 。
【答案】(1)①不溶于水,浅绿色固体(或其它合理答案)
②Cu2(OH)2CO3+2H2SO4=2CuSO4 +CO2↑+3H2O CuSO4 +Fe=FeSO4+Cu(或其它合理答案)
(2)(100-3a)% 或 (1-3a%)×100% 或 (1-3a%)
【解析】
试题分析:根据题中的叙述可知(1)①碱式碳酸铜的物理性质之一是①不溶于水,浅绿色固体等;②用稀硫酸、铁为原料将碱式碳酸铜转化为铜,根据所学物质的性质可知碱式碳酸铜与硫酸反应生成硫酸铜,硫酸铜中加入金属铁,发生置换,故反应的化学方程式是:Cu2(OH)2CO3+2H2SO4=2CuSO4 +CO2↑+3H2O CuSO4 +Fe=FeSO4+Cu;
(2)根据组成固定的原则可知,在硫酸铁和硫酸亚铁组成的混合物中,硫元素和氧元素的质量比为:32:(16×4)=1:2,由于混合物中硫元素的质量分数为a%,所以氧元素的质量分数为2a%,故铁元素的质量分数为:1-3 a %

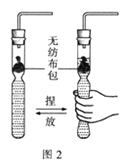
【题目】(10分)在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
探究一 M溶液中的溶质是什么?
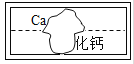
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:①是 ,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
实验操作 | 实验现象 | 实验结论 |
取少量M溶液于试管中,向其中滴加 | 猜想①正确,碳酸钠与其反应的化学方程式为 |
探究二 过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH和Na2CO3;猜想二:_____;猜想三:NaOH
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
取样于试管中,滴入几滴稀盐酸 | 没有气体产生 | “猜想一”不成立 |
他们的实验结论是否正确? ,理由是 .
(4)【继续探究】设计实验方案确定滤液中溶质的组成.
实验操作 | 实验现象 | 实验结论 |
分别取少量滤液于A、B两支试管中,A中加入CaCI2溶液,B中加入 溶液 | 若A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
“猜想二”成立 | ||
“猜想三”成立 |