��Ŀ����
������������õ����յȹ�Ч�����������ϲ����������ʾ�������к�̼���80��93%��������4��14%��ˮ��2��4%��ʮ���ְ����ᡢ28����Ԫ�أ�Ȼ��һЩ���������û��յı��Ǽ��Ϲ�ҵ�������������Ƶ�ҩˮ������ϴ����ɹ�Ժ�ֱ�Ӽӹ����ۣ�����Ҫ�ɷ��ǣ�̼��ƣ������������������ƣ�������ij��ѧ��ȤС����Ʊ��������飬���ⶨ������̼��ƺ�����ʵ��̽��������
��̽��һ�����������������١�
����ֱ�����ˮ����ֽ��衢���ã��ⶨ�ϲ���Һ��pH����pH�� ��7�������������=����Ϊ�����飬�������� ����
��̽�������ⶨ������̼��ƺ�����
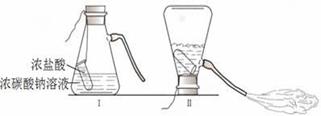
С������ͼ��ʾװ�òⶨ���������̼��Ƶĺ�����ʵ�鷽�����£�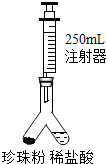
��1�����װ�������ԣ���ͼ1����װ���ú�ע�������������Ϊ250mL�������ǻ�����Ħ�������أ���ͬ���ӿ̶�10mL�����������̶�20mL������ ��������������������������ã���2����ͼ1����װ�������װ��1.1g �����������Ʒ���ҹ��ڵ���һ������ϡ���ᣬע���������Ƶ��ײ����ٴ�����װ�ã�
��3���跨ʹ���������ڵ�ҩƷ��ϣ���Ӧ�������ȡע��������Ϊ220mL��
��4�����ݴ���������ø��������̼��Ƶ���������Ϊ�� ����[�ѡ�CO2����2g/L���������С�����1λ]
��ʵ��˼��������1����ʵ���еķ�Ӧԭ������ �����û�ѧ����ʽ��ʾ����
��2������ע�������أ���ʵ�鷽��������۵����������Ƿ������Ҫ���� ����
��3����̽�������еĵڣ�3�������������ҩƷ�ķ������� ����
��4����ʵ��װ������ϵ��ŵ������� ����д��1�㼴�ɣ���
��̽��һ�������������в�����������ʹ����Һ�ʼ��ԣ�
��̽��������1���ɿ�ע�����������������»ص�10mL�̶ȴ�����4��90.9%��
��ʵ�鷴˼����1��CaCO3+2HCl��CaCl2+H2O+CO2����
��2����Ҫ�������������̫������CO2������������ע�����������ƣ�����������
��3��������װ��������б��ʹϡ����������߹��ڣ���4����������Ͳ�����������
���������������������ṩ����Ϣ���з�����������ijɷ��к����������ƣ�ʹ��ˮ��Һ�ʼ��ԣ����ݲ����Ķ�����̼�����������Լ������Ʒ��̼��Ƶ�������������������Ķ�����̼�����������ע�����IJ�����Χ���������вⶨ������Ʒ��������Ҫ���ƣ��ݴ˽�ɡ�
��̽��һ���������к����������ƣ�ʹ��Һ�ʼ��ԣ�pH����7����������������в�����������ʹ����Һ�ʼ��ԣ�
��̽��������1����װ�����������ã���ע���������������ɿ���ʱ���������»ص�ԭ����λ�ã�����ɿ�ע�����������������»ص�10mL�̶ȴ���
��4��ע��������Ϊ220mL�������ɵĶ�����̼������Ϊ��0.22L��2g/L��0.44g����̼��Ƶ�����Ϊx
CaCO3+2HCl��CaCl2+H2O+CO2��
100 44
x 0.44g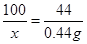
���x��1g
����������̼��Ƶ���������Ϊ��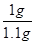 ��100%��90.9%�����90.9%��
��100%��90.9%�����90.9%��
��ʵ�鷴˼����1����ʵ���ԭ��������̼�����ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼�����CaCO3+2HCl��CaCl2+H2O+CO2����
��2����������Ķ�����̼�����������ע�����IJ�����Χ���������вⶨ������Ʒ��������Ҫ���ƣ������Ҫ�������������̫������CO2������������ע�����������ƣ�����������
��3��ΪʹҩƷ��ϣ����Խ�װ��������б��������������߹ع��ڣ����������װ��������б��ʹϡ����������߹��ڣ�
��4����ƴ�ʵ��װ�ã������ڲ������ɵĶ�����̼������������������Ͳ�����������
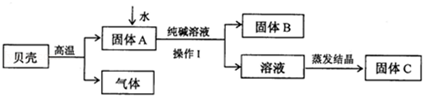
���㣺����ʵ��̽�����ʵ���ɳɷ��Լ�����

ij��ѧ̽��С���ͬѧ����̼������Һ��ʯ��ˮ��Ӧ����ȡ�������ơ�����������һ��̤��ʵ��֮�á�
��1��ʵ����̣��ٰ�ʯ��ˮ����ʢ��̼������Һ���ձ��г�ֽ��裬������Ӧ�Ļ�ѧ����ʽ�� ��
�ڹ��˺���ɫ��Һ�����ᾧ���õ���ɫ���塣
��2�����룺�õ��İ�ɫ�����Ǵ�������������λͬѧ�ֱ��������²��룺
С��Ǵ������������ƣ�
�Ѽѣ����ܻ�����̼���ƣ�
Сǿ��Ҳ���ܺ��� ��
��3����֤��������֤�ѼѵIJ��롣
| ʵ����� | ʵ������ | ʵ����� |
| ȡ������ɫ���������Һ���������� �� | �� | �� |
С�������������к�����������Һ����ʵ��ʱ���μ�����ǰ���˼���ָʾ�����������жϸ��кͷ�Ӧ���еij̶ȡ���������������Һ������Խ���̽����
��̽��Ŀ�ġ�̽��������Һ�������
��������롿������Һ���ܳʼ��ԣ�Ҳ���ܳ� �ԣ������ܳ� �ԡ�
��ʵ����֤��
| ʵ����� | ʵ������ | ���� |
| ���Թ�ȡ����Һ1-2mL������1-2����ɫ��̪��Һ���� | ��ɫ��̪��Һ�� | ��Һ�ʼ��� |
| ��ɫ��̪��Һ����ɫ | ��Һ�� |
��������˼����
��1������Һ�ʼ��ԣ�����Һ��ʹ��ʼ��Ե������� ����д�����ţ���Ϊ���������Һ��Ⱦ������С����������Һ���������´���������Һ����μ��� ��Һ��ֱ�����ٲ�������Ϊֹ��Ȼ����ˣ�����Һ�����������м��ȣ��õ��Ȼ��ƾ��壬�ù����漰�Ļ�ѧ����ʽΪ ��
��2������ɫ��̪��Һ����ɫ��Ϊ�˽�һ��ȷ����Һ������ԣ�С����������·�����
����һ��ȡ��������̼������Һ�����۲쵽 ������ȡ��Һ�����ԣ�������������������ԡ�
��������ȡ�����������п���������ݲ���������ȡ��Һ�����ԣ��÷�Ӧ�Ļ�ѧ����ʽΪ
��������������������ԡ�
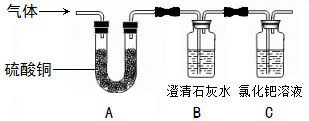
Ϊ��̽������Զ���Һ����ø�����õ�Ӱ�죬С����������ˮ��1%������Һ��ϡ�͵���Һ��ϡ���ᡢ����������Һ����Һ�Ȳ��Ͻ���ʵ�飮���������Ӧ��ʵ����ƺ����������
��ʵ����ơ�
| ʵ����� | ���Ҫ�� |
| ����һ��ȡ3 ֧�ྻ���Թܱ�ΪA��B��c���ڸ��Թ��зֱ����1%������Һ2��������A �Թܼ���l ����ϡ�����l ������Һ����B�Թܼ���1 ��������������Һ��1 ������Һ����C�Թܼ��� | ���ö���ʵ�� |
| ������� | ����ʵ������ |
| ��������10���Ӻ���3֧�Թ��зֱ����1�ε�Һ���۲���ɫ�仯�� | ��ȡʵ��֤�� |
�������������
��ȷ������С���۲쵽A�Թܳ���ɫ����B�Թ�û�г���Ԥ�ڵ���ɫ�����룺ΪʲôB�Թܲ�����ɫ�����Ʋ����������������Һ���ʻ���B�Թ���Һ�����̫��������ʦ�İ����£���֤ʵ������������Һû�б��ʣ���B�Թ���Һ�����ǿ����������ø�Ĵ����ã������B�Թ�û�г�����ɫ����һ�ֺ����IJ²⣺ ��