题目内容
某校同学在老师的指导下,设计了如下实验装置进行气体制取和性质的探究:
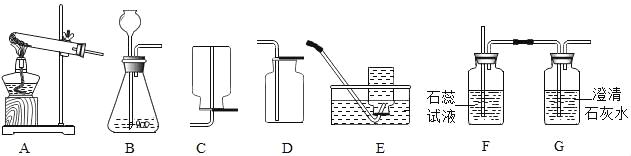
(1)利用图中所示装置,采用以下组合能完成实验室制取气体的有_____(填字母)。
A 用AC制取氧气 B 用BE制取氧气 C 用BD制取氢气 D 用BE制取二氧化碳
(2)若装置B中反应剧烈,从实验安全角度考虑,可以将长颈漏斗换成_____来控制液体的滴加速度;
(3)同学用图中B、F、G装置组合制取二氧化碳气体并验证相关性质。F装置中反应现象是_____;G装置中发生的化学反应方程式为_____。
 学业测评一课一测系列答案
学业测评一课一测系列答案甲醇(CH3OH)可由CO和H2在一定条件下反应制得。原料气(CO和H2)中混有一定量的CO2会对CH3OH产率产生影响。控制其他条件相同,以CO、H2和CO2为原料气进行实验,数据见下表:
实验组别 | 第一组 | 第二组 | 第三组 | ||||||||
原料气体积分数/% | CO2 | 0 | 0 | 0 | 2 | 2 | 2 | 4 | 4 | 4 | |
CO | 30 | 30 | 30 | 28 | 28 | 28 | 26 | 26 | 26 | ||
H2 | 70 | 70 | 70 | 70 | 70 | 70 | 70 | 70 | 70 | ||
反应温度/℃ | 225 | 235 | 250 | 225 | 235 | 250 | 225 | 235 | 250 | ||
CH3OH产率/% | 4.9 | 8.8 | 11.0 | 36.5 | 50.7 | 68.3 | 19.0 | x | 56.5 |
(1)反应中涉及的物质属于有机物的是_____(填字母编号)。
A CH3OH B CO2 C CO D H2
(2)表中x的数值是_____(填字母编号)。
A 11 B 33.1 C 62.1 D 68.3
(3)分析表中数据可知,最佳的实验条件是第_____组、温度为_____℃。
(4)由上表数据可得出多个结论。
结论一:原料气含少量CO2有利于提高CH3OH产率,CO2含量过高反而会降低CH3OH产率。
结论二:_____。
如表除杂质的方法不正确的是( )
选项 | 物质(括号内为杂质) | 除杂方法 |
A | CaO (CaCO3) | 高温煅烧 |
B | NaCl溶液(Na2CO3) | 加入适量的稀盐酸 |
C | CaCl2溶液(HCl) | 加入过量的CaCO3,再过滤 |
D | CO2(HCl) | 先通过足量NaOH溶液,再通过浓硫酸 |
A. A B. B C. C D. D
某同学将氢氧化钠溶液滴入到一定量的稀氯化铜溶液中,出现蓝绿色不溶于水的固体。该同学对生成蓝绿色而不是蓝色固体的现象产生疑惑。
(查阅资料)
(1)CuCl2溶液与NaOH溶液反应可生成蓝色固体(Cu(OH)2),在氢氧化钠较少的情况下会生成蓝绿色碱式氯化铜(Cux(OH)yClz),其不溶于水,能与酸反应。
(2)Cu(OH)2在60℃开始分解生成两种氧化物,100℃分解完全。碱式氯化铜在300℃开始分解生成氧化铜、水和氯化氢,在400℃分解完全。
(猜测)蓝绿色固体可能是:①Cu(OH)2;②Cux(OH)yClz晶体;③___。
猜想①的理由是:___(用化学方程式表示)。
(实验)该同学取31.25g蓝绿色固体,加热至100℃出现黑色固体。则猜想___不正确。继续加热到400℃至质量不再改变,并使产生的气体全部缓缓通过如图___(选填“甲”或“乙”)装置(装置中药品足量)。
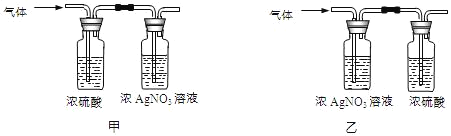
实验数据:①最终得到剩余固体24.00g;
②与硝酸银溶液反应得到的沉淀经过滤、洗涤和低温烘干,得到固体14.35g;
加热前 | 100℃ | 400℃ |
250.00g | 251.80g | 253.60g |
③浓硫酸装置中数据如表。
(延伸)
(1)碱式氯化铜常作为动物饲料的添加剂,则该碱式氯化铜与胃液发生反应的化学方程式为___。
(2)为使实验中生成蓝色固体,少出现蓝绿色固体,应作___改进(选填序号)。
a.实验中将氯化铜溶液滴加到氢氧化钠溶液中
b.实验中应提供足量、较浓的氢氧化钠溶液
c.实验应该在80℃的水浴中进行

