题目内容
【题目】取CaCl2和CaCO3的混合物12.5g于烧杯中,向其中滴加一定溶质质量分数的稀盐酸,滴加稀盐酸的质量与产生气体质量的关系如图所示。求:
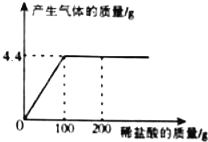
(1)混合物中CaCO3的质量为____g;
(2)恰好完全反应时,所得不饱和溶液中溶质的质量分数?(写出计算过程,计算结果精确到0.1%)
【答案】(1)10;(2)12.6%
【解析】(1)混合物中的碳酸钙与稀盐酸反应生成二氧化碳气体,气体质量是4.4g,设混合物中碳酸钙的质量是x,生成氯化钙的质量是y
CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
100 111 44
x y 4.4g
![]() =
=![]() 解得x=10g
解得x=10g ![]() =
=![]() 解得y=11.1g
解得y=11.1g
恰好完全反应时用去100g稀盐酸,反应后溶液的质量是:12.5g+100g-4.4g=108.1g
溶液中溶质的质量是:(12.5g-10g)+11.1g=13.6g
恰好完全反应时,所得不饱和溶液中溶质的质量分数为: ![]() ×100%=12.6%
×100%=12.6%

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】下列事实的解释合理的是
事 实 | 解 释 | |
A | 淀粉没有甜味 | 淀粉不属于糖类 |
B | 打开汽水瓶盖时,汽水会自动喷出来 | 压强减小,气体在水中的溶解度变小 |
C | 洗洁精可以去除油污 | 洗洁精溶解了油污 |
D | 过滤时使用玻璃棒 | 玻璃棒起搅拌作用 |
A. A B. B C. C D. D
【题目】下列有关“物质性质—类别—用途”的对应关系中正确的是( )
选项 | 物质性质 | 类别 | 用途 |
A | 氢氧化钠具有腐蚀性 | 化学性质 | 制作叶脉书签 |
B | 液氮气化时会吸热 | 物理性质 | 用作保护气 |
C | 生石灰遇水放热 | 物理性质 | 用作干燥剂 |
D | 活性炭具有吸附性 | 化学性质 | 用于制糖工业脱色 |
A. A B. B C. C D. D