题目内容
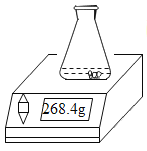
【题目】用久的热水瓶内胆有一层水垢(主要成分是CaCO3和Mg(OH)2)。兴趣小组为了解具体成分进行了实验。他们取样品25克放入质量为100克的锥形瓶中,置于电子天平上,往瓶内加入150克稀盐酸时,恰好完全反应(样品中的杂质不与稀盐酸反应),此时天平示数如图。对所得混合物进行过滤、洗涤、干燥、称量,得到固体4.2克。请回答下列问题:
(1)恰好完全反应时,溶液中的溶质为_____(填化学式)。
(2)样品中CaCO3的质量分数是_______?
(3)反应结束时溶液中MgCl2的质量分数是___________?(精确到0.1%)。
【答案】CaCl2和MgCl2 60% 5.8%
【解析】
(1)恰好完全反应时,碳酸钙转化为氯化钙,氢氧化镁转化为氯化镁,所以对应的溶质的化学式为 CaCl2和MgCl2。故填:CaCl2和MgCl2。
(2)根据质量守恒定律可得,生成的二氧化碳的质量为25g+100g+150g﹣268.4g=6.6g。
设碳酸钙的质量为x。
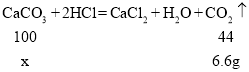
![]()
x=15g
样品中CaCO3的质量分数为![]() ×100%=60%。故填:60%
×100%=60%。故填:60%
(3)样品中氢氧化镁的质量为25g﹣15g﹣4.2g=5.8g。
设生成的氯化镁的质量为y。
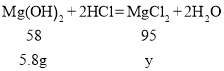
![]()
y=9.5g
反应结束时溶液中MgCl2的质量分数为![]() ×100%
×100%![]() 5.8%。故填:5.8%
5.8%。故填:5.8%

练习册系列答案
相关题目
【题目】对下列实验现象的解释错误的是
A | B | C | D | |
实验现象 |
用扫描隧道显微镜获得的分子图像 |
品红加入水中后,整个液体变红色 |
水分子在不同温度下的运动情况 |
50mL水与50mL酒精混合后的体积小于100mL |
解释 | 分子的质量和体积都很小 | 分子总是不断的运动着的 | 常温时分子不运动,加热时分子才运动 | 分子有空隙 |
A.AB.BC.CD.D