题目内容
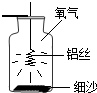 小强同学经过查阅资料得知:铝丝和铁丝一样,也能在氧气中燃烧,于是设计了如图所示的装置进行实验探究,请你结合实验过程回答下列问题.
小强同学经过查阅资料得知:铝丝和铁丝一样,也能在氧气中燃烧,于是设计了如图所示的装置进行实验探究,请你结合实验过程回答下列问题.(1)集气瓶底预先铺少量沙子的目的是
(2)铝丝在空气中不能被点燃,引燃铝丝的办法是:
(3)用正确方法引燃铝丝,伸入装有氧气的集气瓶中后,未观察到铝丝发生剧烈燃烧现象,可能的原因是
考点:氧气的化学性质
专题:氧气、氢气的性质与用途
分析:由于铝丝和铁丝一样,根据铁丝在氧气中燃烧的现象和反应注意事项来回答本题.
解答:解:(1)铝丝燃烧的生成物温度很高,溅落到集气瓶底部容易炸裂,所以集气瓶底预先铺少量沙子,故填:防止生成物掉落下来,炸裂瓶底;
(2)铝丝在空气中不能被点燃,引燃铝丝的办法与铁丝引燃的方法相同,方法是:在铝丝的一端绑上一根火柴,点燃火柴,待火柴快燃尽时伸入氧气瓶中;
(3)未观察到铝丝发生剧烈燃烧现象,可能是:铝丝表面有一层氧化膜未除去或氧气不纯,氧气不纯等.
故答为:(1)防止生成物掉落下来,炸裂瓶底;(2)在铝丝的一端绑上一根火柴,点燃火柴,待火柴快燃尽时伸入氧气瓶中;(3)铝丝表面有一层氧化膜未除去,氧气不纯等
(2)铝丝在空气中不能被点燃,引燃铝丝的办法与铁丝引燃的方法相同,方法是:在铝丝的一端绑上一根火柴,点燃火柴,待火柴快燃尽时伸入氧气瓶中;
(3)未观察到铝丝发生剧烈燃烧现象,可能是:铝丝表面有一层氧化膜未除去或氧气不纯,氧气不纯等.
故答为:(1)防止生成物掉落下来,炸裂瓶底;(2)在铝丝的一端绑上一根火柴,点燃火柴,待火柴快燃尽时伸入氧气瓶中;(3)铝丝表面有一层氧化膜未除去,氧气不纯等
点评:熟记铁丝与铝丝在氧气中燃烧的现象是解决本题的关键.

练习册系列答案
相关题目
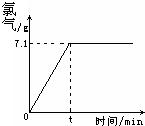 取氯化钠溶液117g进行电解,反应的化学方程式为:2NaCl+2H2O═Cl2↑+H2↑+2NaOH,生成氯气的质量与时间的关系如图所示.请计算:
取氯化钠溶液117g进行电解,反应的化学方程式为:2NaCl+2H2O═Cl2↑+H2↑+2NaOH,生成氯气的质量与时间的关系如图所示.请计算: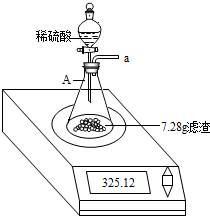 一化学兴趣小组对某月饼包装盒中的“脱氧剂”很好奇,他们观察到“脱氧剂”外包装标注的成分为铁粉、活性炭和氯化钠,打开发现灰黑色的固体中还夹杂着少量红棕色粉末.
一化学兴趣小组对某月饼包装盒中的“脱氧剂”很好奇,他们观察到“脱氧剂”外包装标注的成分为铁粉、活性炭和氯化钠,打开发现灰黑色的固体中还夹杂着少量红棕色粉末.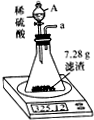
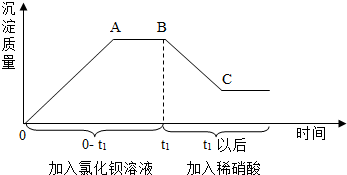 某溶液中可能含有碳酸钠、硫酸钠、氯化钠、硝酸钠中的一种或几种,为测定其成分,进行如下实验.取样,先后逐滴加入氯化钡溶液、稀硝酸,产生沉淀的质量与时间的关系如图所示.
某溶液中可能含有碳酸钠、硫酸钠、氯化钠、硝酸钠中的一种或几种,为测定其成分,进行如下实验.取样,先后逐滴加入氯化钡溶液、稀硝酸,产生沉淀的质量与时间的关系如图所示.