题目内容
【题目】中招实验考试之前,小明从实验室里拿出一瓶密封保存的溶液。
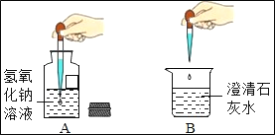
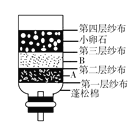
(1)如 A 图所示练习吸取液体的操作。请纠正该同学操作中的错误之处_________。
(2)练习一段时间后,他把瓶中溶液滴入盛有澄清石灰水的烧杯中(如 B图所示),发现产生白色沉淀,请用化学方程式解释产生沉淀的原因______________________。
【答案】使用滴管吸取液体时,应先挤压橡胶胶帽,再伸入液面下松开胶帽。CO2+2NaOH=Na2CO3+H2O Na2CO3+Ca(OH)2= CaCO3↓+2NaOH
【解析】
(1)根据图示可以看出,该同学向氢氧化钠溶液中挤入了空气,应该是在使用滴管吸取液体时,应先挤压橡胶胶帽,再伸入液面下松开胶帽;
(2)氢氧化钠能与二氧化碳反应生成碳酸钠和水,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:2NaOH+CO2═Na2CO3+H2O、Ca(OH)2+Na2CO3═CaCO3↓+2NaOH。

【题目】某小组同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行探究。
(提出问题)①三种溶液的酸碱性?②它们与酸反应时溶液的pH如何变化?
(查阅资料)
pH | 2~3 | 4~6 | 7 | 8~9 | 10~11 | 12~14 |
紫甘蓝汁液显示的颜色 | 紫红 | 浅紫 | 紫色 | 蓝色 | 绿色 | 黄色 |
(实验1)向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 | 蒸馏水 | 碳酸氢钠溶液 | 碳酸钠溶液 | 氢氧化钠溶液 |
紫甘蓝汁液显示的颜色 | 紫色 | 蓝色 | 绿色 | 黄色 |
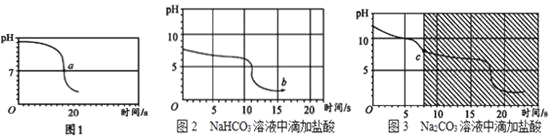
(实验2)向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图1所示。
(实验3)向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图2、图3所示。将图2与图3的阴影部分进行叠加,发现两者基本重合。
(解释与结论)
(1)实验1得出三种溶液中碱性最强的为______________溶液。
(2)实验2证明了氢氧化钠能与盐酸发生反应,其理由是______________,该反应的化学方程式为______________。若取出少量a点的溶液,向其中滴加紫甘蓝汁液,观察到的现象是______________。
(3)实验3中,b点的溶质为______________,实验3中,c点后发生反应的化学方程式为_____________。
(4)依据实验3,加入足量的盐酸,产生二氧化碳的量______________。
A.碳酸氢钠多 B.碳酸钠多
C.两者一样多 D.不能确定哪个多