题目内容
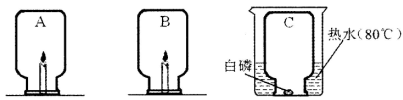
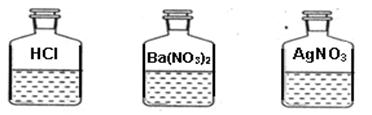
实验室中有一瓶标签破损的固态铵盐,它可能是NH4Cl、NH4NO3、NH4HCO3、(NH4)2SO4中的一种,请利用下图所示的溶液进行实验探究。
【提出猜想】猜想①:该铵盐是NH4Cl
猜想②:该铵盐是
猜想③:该铵盐是NH4HCO3
猜想④:该铵盐是(NH4)2SO4
【实验探究】
步骤一:取少量样品放入试管中,没有嗅到强烈的氨味,加入适量水溶解得到无色液体,选用图中的 溶液滴入试管中,无气泡放出,则猜想③不成立。
步骤二:在步骤一所得的溶液中,滴加图中的Ba(NO3)2溶液,没有白色沉淀生成,则猜想 不成立。
步骤三:另取适量样品放入试管中,加水溶解配成溶液,滴加图中的 溶液,有白色沉淀生成,则猜想 成立。
【拓展应用】铵盐可作氮肥,它会与碱性物质发生化学反应,请写出硝酸铵溶液与氢氧化钠溶液在加热条件下反应的化学方程式 ,所以在农业生产中,为避免降低肥效,铵态氮肥不要与碱性物质混合施用。

【提出猜想】猜想①:该铵盐是NH4Cl
猜想②:该铵盐是
猜想③:该铵盐是NH4HCO3
猜想④:该铵盐是(NH4)2SO4
【实验探究】
步骤一:取少量样品放入试管中,没有嗅到强烈的氨味,加入适量水溶解得到无色液体,选用图中的 溶液滴入试管中,无气泡放出,则猜想③不成立。
步骤二:在步骤一所得的溶液中,滴加图中的Ba(NO3)2溶液,没有白色沉淀生成,则猜想 不成立。
步骤三:另取适量样品放入试管中,加水溶解配成溶液,滴加图中的 溶液,有白色沉淀生成,则猜想 成立。
【拓展应用】铵盐可作氮肥,它会与碱性物质发生化学反应,请写出硝酸铵溶液与氢氧化钠溶液在加热条件下反应的化学方程式 ,所以在农业生产中,为避免降低肥效,铵态氮肥不要与碱性物质混合施用。
【提出猜想】猜想②:NH4NO3
【实验探究】步骤一:稀盐酸(或HCl溶液)
步骤二:④
步骤三:硝酸银 ①
【拓展应用】NH4NO3 + NaOH="==" NaNO3 + H2O + NH3↑
【实验探究】步骤一:稀盐酸(或HCl溶液)
步骤二:④
步骤三:硝酸银 ①
【拓展应用】NH4NO3 + NaOH="==" NaNO3 + H2O + NH3↑
试题分析:它可能是NH4Cl、NH4NO3、NH4HCO3、(NH4)2SO4中的一种,其余三种猜想已给出,所以猜想②是NH4NO3.
【实验探究】步骤一:根据取少量样品放入试管中,没有嗅到强烈的氨味,加入适量水溶解得到无色液体,滴入这种溶液无气泡放出,说明该样品中不含碳酸氢铵.故答案:稀盐酸(或HCl).步骤二:NH4Cl、NH4NO3、NH4HCO3、(NH4)2SO4中只有(NH4)2SO4能和硝酸钡反应生成白色沉淀,其余三种都不能和硝酸钡反应.故答案:④.步骤三:稀盐酸和硝酸钡都用过了只有硝酸银没有用,且硝酸银和硝酸铵不反应,但和氯化铵反应生成氯化银白色沉淀和硝酸铵,故答案:硝酸银 ①.
【拓展应用】硝酸铵溶液与氢氧化钠溶液在加热条件下反应,生成硝酸钠、氨气和水,故答案:NH4NO3+NaOH=NaNO3+NH3↑+H2O
点评:本题综合考查了铵盐的化学性质,只要熟练掌握复分解反应和硫酸钡、氯化银是白色沉淀不难解答该题。

练习册系列答案
相关题目