题目内容
【题目】下图中是初中化学常见的一些物质,A是石灰石的主要成分,K是最常用的溶剂,D是胃酸的主要成分,E是金属单质,F是金属氧化物,G溶液呈浅绿色,J溶液呈蓝色,物之间的转化关系如下图:
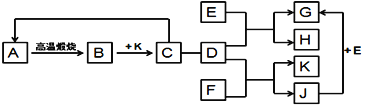
(1)请根据已知条件推断下列物质的化学式:
H是______;E是___________;
(2)请写出下列反应的化学方程式:
C ![]() A:____________________________________
A:____________________________________
D + F ![]() K + J:___________________________
K + J:___________________________
J + E ![]() G:_________________________ ;该反应的现象为______________ 。
G:_________________________ ;该反应的现象为______________ 。
【答案】 H2 Fe Ca(OH) 2+CO2 =CaCO3↓+H2O CuO+2HCl==CuCl2 +H2O Fe+ CuCl2 =FeCl2+Cu 有红色物质生成,溶液由蓝色变为浅绿色
【解析】本题是框图型推断题。在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
A是石灰石的主要成分,则A是碳酸钙,碳酸钙高温煅烧生成氧化钙和二氧化碳,K是最常用的溶剂,则K是水,B与水生成C,C可能为氢氧化钙或碳酸,C能转化为碳酸钙,则C为氢氧化钙,B为氧化钙; D是胃酸的主要成分,则D是盐酸,盐酸与E反应生成G与H,E是金属单质,G溶液呈浅绿色,则E是铁,G是氯化亚铁,H是氢气;盐酸与F反应生成水和J,F是金属氧化物, J溶液呈蓝色,则F为氧化铜,J为氯化铜, 氯化铜与铁反应能生成氯化亚铁,代入框图,推理合理。因此:
(1)H是氢气,化学式是:H2;E是铁,化学式是Fe;
(2)C![]() A可以是氢氧化钙与二氧化碳反应生成碳酸钙和水,反应的化学方程式是:Ca(OH) 2 + CO2 ==CaCO3 ↓ + H2O;
A可以是氢氧化钙与二氧化碳反应生成碳酸钙和水,反应的化学方程式是:Ca(OH) 2 + CO2 ==CaCO3 ↓ + H2O;
D + F![]() K + J是氧化铜与盐酸反应生成水和氯化铜,反应化学方程式是:CuO + 2HCl == CuCl2 + H2O;
K + J是氧化铜与盐酸反应生成水和氯化铜,反应化学方程式是:CuO + 2HCl == CuCl2 + H2O;
J + E![]() G是氯化铜与铁反应生成氯化亚铁,反应的化学方程式是:Fe+ CuCl2 == FeCl2 + Cu;该反应的现象为有红色物质生成,溶液由蓝色变为浅绿色。
G是氯化铜与铁反应生成氯化亚铁,反应的化学方程式是:Fe+ CuCl2 == FeCl2 + Cu;该反应的现象为有红色物质生成,溶液由蓝色变为浅绿色。

【题目】实验室有一瓶标签腐蚀的溶液A(如图),某组同学将碳酸钠溶液与样品反应,有白色沉淀产生,过滤后得到澄清滤液,同学们进行了一系列的探究。

探究一:A溶液中溶质是什么?
【提出猜想】①CaCl2,②_________________。
【查阅资料】CaCl2溶液呈中性。
【设计实验】同学们设计了如下方案并进行实验。
实验操作 | 实验现象 | 实验结论 |
取少量A溶液于试管中,向其中滴加无色酚酞溶液 | _______________________ | 猜想①正确 |
碳酸钠与其反应的化学方程式为_______________________________________。
探究二:过滤后的滤液中会有哪些溶质?
【提出猜想】小明的猜想:NaCl、CaCl2;
小红的猜想:NaCl;
你的猜想:_________________________。
【设计实验】请设计对“你的猜想”实验:
实验步骤 | 实验现象 | 实验结论 |
_______ | ___________ | 你的猜想正确 |