题目内容
【题目】利用电石渣[主要成分为Ca(OH)2、MgO]制备硫酸钙的主要工艺流程如下:
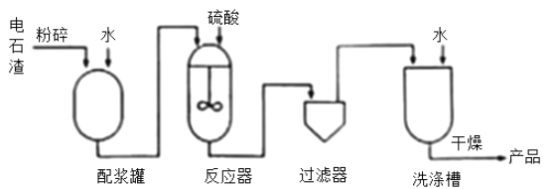
己知:MgO难溶于水;MgSO4易溶于水;CaSO4微溶于水。
(1)反应器中搅拌的目的是__________________________________________________。
(2)反应器中发生的反应主要有MgO+H2SO4=MgSO4+H2O和____________________。
(3)上述流程中,用于分离提纯的设备有______________________________________。
【答案】使反应物充分接触,加快反应速率,反应更充分 Ca(OH)2+H2SO4=CaSO4![]() +2H2O 过滤器和洗涤槽
+2H2O 过滤器和洗涤槽
【解析】
(1) 反应器中搅拌的目的是使反应物充分接触,加快反应速率,反应更充分;
(2) 反应器中发生的主要反应除了氧化镁和稀硫酸外,还有氢氧化钙和稀硫酸反应生成微溶物硫酸钙和水,化学方程式为:Ca(OH)2+H2SO4=CaSO4![]() +2H2O;
+2H2O;
(3)由图可知,用于分离提纯的设备有过滤器和洗涤槽。

【题目】材料一:候德榜是我国著名的化学家,发明了侯氏制碱法,为纯碱和氮肥工业技术的发展作出了杰出的贡献。下面是实验室模拟侯氏制碱法原理的生产过程:

①20℃时,将CO2通入含NH3的饱和NaCl溶液中,生成 NaHCO3晶体和NH4Cl溶液。
②将①中的产物 NaHCO3晶体充分加热分解,得到Na2CO3、H2O和CO2。
材料二:20℃时几种物质在水中的溶解度/g
NaCl | NH4Cl | NaHCO3 |
36.0 | 37.2 | 9.6 |
请回答下列问题:
(1)在第①步反应中,有 NaHCO3晶体析出,而没有NH4Cl和NaCl晶体析出的原因是_____。
(2)该生产过程中部分生成物可作为原料循环使用的是_____,同时得到的副产品NH4Cl是一种氮肥。
【题目】下图“黑面包”实验中,蔗糖(C12H22O11)变黑,体积膨胀,变成疏松的炭,放出有刺激性气味的气体。

(提出问题)改变糖的种类、浓硫酸的体积、水的滴数和温度是否会影响实验效果呢?
(进行实验)分别取5g糖粉进行实验,根据前2min的现象对实验效果进行评分,
记录如下:
表1实验记录
实验 | 糖 | 浓硫酸体积/mL | 水的滴数 | 温度/℃ | 效果得分 |
1 | 蔗糖 | 4 | 5 | 22 | 65 |
2 | 蔗糖 | 5 | 10 | 30 | 81 |
3 | 蔗糖 | 6 | 15 | 50 | 93 |
4 | 冰糖 | 4 | 10 | 50 | 91 |
5 | 冰糖 | 5 | 15 | 22 | 88 |
6 | 冰糖 | a | 5 | 30 | 75 |
7 | 葡萄糖 | 4 | 15 | 30 | 0 |
8 | 葡萄糖 | 5 | 5 | 50 | 0 |
9 | 葡萄糖 | 6 | 10 | 22 | 0 |
(处理数据)分析表1,计算效果得分均值,结果如下:
表2效果得分均值
因素 | 糖 | 浓硫酸体积/mL | 水的滴数 | 温度/℃ | ||||||||
蔗糖 | 冰糖 | 葡萄糖 | 4 | 5 | 6 | 5 | 10 | 15 | 22 | 30 | 50 | |
均值 | 79.7 | 84.7 | 0 | 52.0 | 56.3 | 56.0 | 46.7 | 57.3 | 60.3 | 51.0 | 52.0 | 61.3 |
依据均值推断最佳实验方案,均值越高,效果越好。
(解释与结论)
(1)蔗糖变成黑色的炭,发生了_____________(填“物理”或“化学”)变化。
(2)推测放出的气体含SO2,从元素守恒角度说明理由:________________________________。
(3)实验6中,a为_____________mL。
(4)根据表2推断,“黑面包”实验最好选择5g冰糖、5mL浓硫酸、_____滴水和50℃
(反思与评价)
(5)表2中,22℃对应的均值为51.0,计算该值所依据的3个数据分别是_____________________。
(6)综合分析,使实验3的效果得分高于实验4的因素有________________________________。