题目内容
小红同学在实验室做实验时,不小心将酚酞试液滴入碳酸钠溶液的试管中.发现溶液的颜色变红了。她觉得很奇怪,又做了以下工作:
实验一:重新取一洁净的试管和纯净的碳酸钠溶液,滴加酚酞试液,酚酞试液变红;用pH试纸测试,溶液的pH=11。
实验二:分别测试纯净碳酸钾、氯化钠、硫酸铜、硫酸钠、氯化铁、硝酸钾溶液的pH,实验结果如表:
| 盐 | K2CO3 | NaCl | CuSO4 | Na2SO4 | FeCl3 | KNO3 |
| pH | 10 | 7 | 4 | 7 | 3 | 7 |
她还到图书馆查阅了有关资料,得到如下信息:酸和碱都有强弱之分,盐酸、硫酸、硝酸是强酸,碳酸、醋酸等是弱酸。氢氧化钠、氢氧化钾是强碱,氢氧化铁、氢氧化铜是弱碱。
盐是酸碱中和反应的产物,强酸和弱碱反应生成的盐叫强酸弱碱盐,强碱和弱酸反应生成的盐叫强碱弱酸盐。问:
(1)由最开始的实验,你认为溶液变红的原因可能是
(2)她重新进行实验一得出的结论是
(3)由实验二得出的结论是
(4)由实验二及查得的资料进行分析,你还能得出哪几点结论
(1)碳酸钠溶液中含碱溶液,或试管内壁不干净(合理答案也可)
(2)碳酸钠溶液能使酚酞试液变红,碳酸钠溶液pH>7显碱性均可
(3)有的盐溶液pH=7有的pH>7有的pH<7
(4)强酸弱碱盐溶液显酸性,强碱弱酸盐溶液显碱性,强酸强碱盐溶液显中性,或显酸性的溶液不一定是酸,显碱性的不一定是碱

实验探究让化学更具魅力,请帮助完成下列实验探究
(1)同学们在做完“二氧化碳的实验室制取”后,对废液进行了如下处理:过滤,取滤液于烧杯中,逐滴滴入Na2CO3溶液至过量.
记录滴入Na2CO3溶液质量(x)与有关的变化关系如图
所示.图中纵坐标(y)表示_______________,AB段
发生反应的化学方程式是___________________ _____,
_____,
反应进行到A点时,溶液中的溶质是______________,
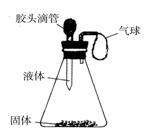 C点时溶液的 pH___ _(填“>”“<”“=”)7.
C点时溶液的 pH___ _(填“>”“<”“=”)7.
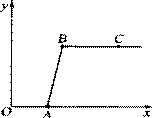 (2)如图所示,一同学挤压胶头滴管中的液体,
(2)如图所示,一同学挤压胶头滴管中的液体,
使之与瓶中固体接触,小气球鼓了起来。
请写出符合这一现象的化学方程式:
①置换反应_____________________ __;
__;
②化合反应_________________________。
(3)实验室中,同学们发现一瓶石灰水试剂瓶瓶壁和瓶塞周围有一些白色粉末.为了弄清楚白色粉末的成分及形成原因,他们进行了如下探究:
①对白色粉末成分的猜想和成因分析:
| 白色粉末的成分 | 形 |
| 可能是CaCO3 | 石灰水与空气中CO2反应: 化学方程式为: |
| 可能是 | 随着气温的升高,溶质的溶解度会 (填变大或变小)或溶剂蒸发,石灰水中的溶质析出 |
经过反复思考,同学们认为白色粉末还可能是以上两种物质的混合物.
②设计实验:甲同学取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解,于是他得出粉末中只有CaCO3的结论。乙同学查阅了溶解性表,认为甲同学的结论不严密,理由是: 。
为了得出较严密的结论,他们进行了如下实验,请完成下列实验报告:
| 实 验 步 骤 | 可能观察到的现象 | 结 论 |
| 取上述试管中的上层清液,滴加1~2滴无色酚酞试液 | 溶液变红 |
|
| 往上述试管内残留的固体中加入 |
| 白色粉末中含有CaCO3 |
③交流与反思
通过上述实验的探究,同学们向实验室提出保存、使用易变质的溶液时的下列建议,合理的是 。A.密封保存 B.使用前,临时配制 (填序号)
 实验探究让化学更具魅力,请帮助完成下列实验探究
实验探究让化学更具魅力,请帮助完成下列实验探究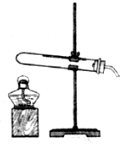 小明暑假期间到农田施肥时,发现撒落在地上的碳铵(碳酸氢铵的简称)在阳光的照射下很快消失了,同时有浓烈的刺激性气味.他很好奇,返校后和同学们进行探究,请你一同参与:
小明暑假期间到农田施肥时,发现撒落在地上的碳铵(碳酸氢铵的简称)在阳光的照射下很快消失了,同时有浓烈的刺激性气味.他很好奇,返校后和同学们进行探究,请你一同参与: