题目内容
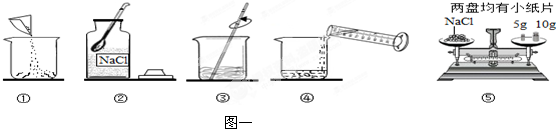
根据如图所示实验,回答下列问题.

(1)A实验中发生反应的化学方程式为
(2)B实验中能得出“可燃物必须与氧气接触”这一燃烧条件的实验现象为
(3)C实验中,应在
(4)通过D实验得出的结论是

(1)A实验中发生反应的化学方程式为
3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
.
| ||
(2)B实验中能得出“可燃物必须与氧气接触”这一燃烧条件的实验现象为
上面的白磷燃烧而水中的白磷不燃烧
上面的白磷燃烧而水中的白磷不燃烧
.(3)C实验中,应在
装置冷却到室温
装置冷却到室温
时打开止水夹.(4)通过D实验得出的结论是
二氧化碳密度比空气大;不燃烧,一般也不支持燃烧
二氧化碳密度比空气大;不燃烧,一般也不支持燃烧
.分析:(1)根据铁丝燃烧的原理结合化学方程式的书写分析;
(2)根据现象分析燃烧的条件;
(3)根据测定空气中氧气的含量的实验注意事项分析;
(4)根据现象分析二氧化碳的性质.
(2)根据现象分析燃烧的条件;
(3)根据测定空气中氧气的含量的实验注意事项分析;
(4)根据现象分析二氧化碳的性质.
解答:解:(1)铁丝燃烧反应的化学方程式为3Fe+2O2
Fe3O4;
(2)上面的白磷燃烧而水中的白磷不燃烧说明“可燃物必须与氧气接触”;
(3)C实验中,为了测量结果更准确,应在装置冷却到室温时打开止水夹;
(4)蜡烛自下至上依次熄灭,说明二氧化碳的密度比空气大;不燃烧,不支持燃烧.
故答案为:(1)3Fe+2O2
Fe3O4;(2)上面的白磷燃烧而水中的白磷不燃烧;(3)装置冷却到室温;(4)二氧化碳密度比空气大;不燃烧,一般也不支持燃烧.
| ||
(2)上面的白磷燃烧而水中的白磷不燃烧说明“可燃物必须与氧气接触”;
(3)C实验中,为了测量结果更准确,应在装置冷却到室温时打开止水夹;
(4)蜡烛自下至上依次熄灭,说明二氧化碳的密度比空气大;不燃烧,不支持燃烧.
故答案为:(1)3Fe+2O2
| ||
点评:本题考查了铁丝的性质、二氧化碳的性质及燃烧条件的探究等,属于基础性的考查,难度不大,要求学生在平时的学习置换要扎实基础.

练习册系列答案
相关题目
 某同学用如图所示的装置在实验室加热高锰酸钾制取氧气,请回答问题:
某同学用如图所示的装置在实验室加热高锰酸钾制取氧气,请回答问题: 某同学用如图所示的装置在实验室加热高锰酸钾制取氧气,请回答问题:
某同学用如图所示的装置在实验室加热高锰酸钾制取氧气,请回答问题: