题目内容
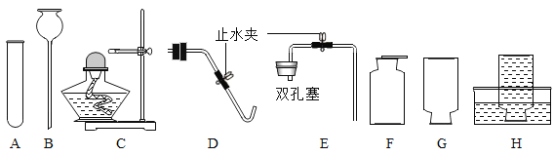
【题目】某校化学兴趣小组的同学利用下列装置进行实验:

[实验目的]:(1)做高锰酸钾钾制取一瓶氧气及细铁丝在氧气中燃烧的实验。
(2)粗略测定加热2g高锰酸钾所收集到的氧气的体积。
[反应原理]:细铁丝在氧气中燃烧的化学方程式是_____,用高锰酸钾制氧气的化学方程式_____。
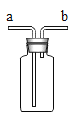
[装置连结]:为了达到实验目的,各装置的正确连接顺序是:(填接口字母)a→_____→_____→d
[问题分析]:(1)实验过程中发现B瓶中的水变红了,原因是_____;
(2)用收集到的氧气做细铁丝燃烧实验时,发现集气瓶底部炸裂,发生该操作失误的原因可能是_____。
(3)根据化学方程式可算出理论上加热2g高锰酸钾,完全分解后可生成氧气的质量是是0.203g。而实际测得制得的氧气在标准状况下的体积为138mL,换算成质量为0.198g,低于理论量0.203g-0.198g=0.005g。你认为实际制得的氧气低于理论量的可能原因是什么?_____(写出一种可能的情况)。
【答案】3Fe+2O2![]() Fe3O4 2KMnO4
Fe3O4 2KMnO4![]() K2MnO4+MnO2+O2↑ c b 试管口未放一团棉花 瓶底未装少量水或铺一层细沙 装置气密性不好。(其它合理答案也可)
K2MnO4+MnO2+O2↑ c b 试管口未放一团棉花 瓶底未装少量水或铺一层细沙 装置气密性不好。(其它合理答案也可)
【解析】
细铁丝在氧气中燃烧生成四氧化三铁,高锰酸钾加热生成锰酸钾、二氧化锰和氧气。
[反应原理]细铁丝在氧气中燃烧生成四氧化三铁,化学方程式为3Fe+2O2![]() Fe3O4,高锰酸钾加热生成锰酸钾、二氧化锰和氧气,故制取氧气的化学方程式为
Fe3O4,高锰酸钾加热生成锰酸钾、二氧化锰和氧气,故制取氧气的化学方程式为
2KMnO4![]() K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。
[装置连结]氧气不易溶于水,用排水法收集,故为了达到实验目的,各装置的正确连接顺序是 a→c→b→d。
[问题分析](1)实验过程中发现B瓶中的水变红了,原因是试管口未放一团棉花,高锰酸钾粉末从导管口喷出。
(2)用收集到的氧气做细铁丝燃烧实验时,发现集气瓶底部炸裂,发生该操作失误的原因可能是瓶底未装少量水或铺一层细沙。
(3)实际制得的氧气低于理论量的可能原因是装置气密性不好。

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案