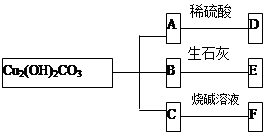题目内容
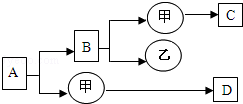
(1)有一种无色液体A通电后产生无色气体B和无色气体C。(2)将紫黑色固体加热能得到B。(3)将银白色的金属丝D放入B中燃烧,火星四射并放出大量的热,生成黑色固体E。(4)将红色固体F放入B中燃烧产生白烟。请写出各步化学反应的化学方程式
(1) ,(2) ,
(3) ,(4) 。
(1)2H2O 2H2↑+O2↑;(2) 2KMnO4
2H2↑+O2↑;(2) 2KMnO4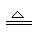 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
(3) 3Fe+2O2 Fe3O4 ; (4) 4P+5O2
Fe3O4 ; (4) 4P+5O2 2P2O5
2P2O5
解析试题分析:根据反应条件是“通电”可知该反应是电解水,A是水;紫黑色固体是高锰酸钾,高锰酸钾分解产生氧气,则B是氧气;银白色的金属丝D放入氧气中燃烧,火星四射并放出大量的热,生成黑色固体E,根据现象可知,D是铁,E是四氧化三铁;红色固体F放入氧气中燃烧产生白烟,则红色固体是红磷,白烟是生产的五氧化二磷。
考点:物质的推断及化学方程式的书写

 桃李文化快乐暑假武汉出版社系列答案
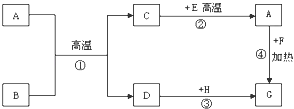
桃李文化快乐暑假武汉出版社系列答案下图表示实验室用稀H2SO4、CuO、Fe粉三种物质,制取铜的两种实验方案。
|
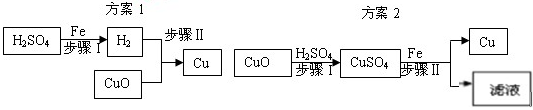 (1)若按方案1制取铜,步骤II反应的现象是 。
(1)若按方案1制取铜,步骤II反应的现象是 。(2)若按方案2制取铜,步骤I发生反应的化学方程式 。
(3)两种方案比较,方案 更好,理由是: 。
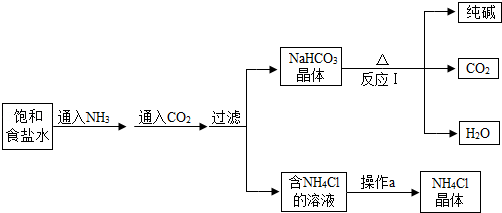
小明发现家中施用的碳酸氢铵(NH4HCO3)减少了,并闻到一股刺激性的气味。他很好奇,于是和同学们进行探究,请你一同参与:
[提出问题] 碳酸氢氨减少的原因是什么?
[猜想假设] 碳酸氢铵受热易分解,产物可能为水、二氧化碳、氨气。
[实验设计] 小明设计了如图所示的装置进行实验 (实验装置中的铁架台省略)。
(1)A装置大烧杯中的生石灰和水的作用是 。
(2)装置B中澄清石灰水 ,证明产物中有二氧化碳生成。
(3)根据现象 ,证明实验后生成了水和氨气。
(4)小红同学认为若将装置B中澄清石灰水改为NaOH溶液,再经过某实验操作,也可以证明碳酸氢铵分解后有二氧化碳生成,请你帮她设计完成实验:
| 实验步骤 | 实验现象 | 反应的方程式 |
| | | |
[实验结论]碳酸氢铵受热易分解,其反应的化学方程式为 。
[实验反思]根据以上实验,你认为是 ,在施用时注意 。
某研究性学习小组为了探究氢氧化钠溶液与稀硫酸是否恰好完全反应,分别取少量反应后的溶液于试管中,用下表中的不同试剂进行实验.下列选项错误的是( )
| 选项 | 所用试剂 | 现象和结论 |
| A | 硫酸铜溶液 | 出现蓝色沉淀,则氢氧化钠过量 |
| B | 氯化钡溶液 | 出现白色沉淀,则硫酸过量 |
| C | 锌粒 | 有气泡产生,则硫酸过量 |
| D | 无色酚酞溶液 | 溶液不变色,则恰好完全反应 |