题目内容
相同质量的H2、CH4和CO,完全燃烧需要氧气的质量( )A.H2最多
B.CH4最多
C.CO最多
D.三者相同
【答案】分析:本题没有数据,为了便于计算和比较,可假定质量都是1克,然后写出化学方程式并计算出氧气的质量,再进行比较即可得出结果.
解答:解:假定质量都1克,设和氢气反应的氧气的质量是X,和甲烷反应的氧气的质量是Y,和一氧化碳反应的氧气的质量是Z.
2H2+O2 2H2O
2H2O
4 32
1克 X
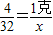 得:X=8克
得:X=8克
CH4+2O2 CO2+2H2O
CO2+2H2O
16 64
1克 Y
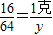 得:Y=4克
得:Y=4克
2CO+O2 2CO2
2CO2
56 32
1克 Z
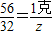 得:Z=0.57克
得:Z=0.57克
通过计算、比较可知,相同质量的H2、CH4和CO,完全燃烧需要氧气的质量最多的是氢气,故A正确,B、C、D错误.
故选A.
点评:本题属于根据化学方程式的计算的无数据题,在计算时为了便于计算和比较,可假定质量都是1克,然后写出化学方程式并计算出氧气的质量,再进行比较即可.
解答:解:假定质量都1克,设和氢气反应的氧气的质量是X,和甲烷反应的氧气的质量是Y,和一氧化碳反应的氧气的质量是Z.
2H2+O2
 2H2O
2H2O4 32
1克 X
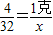 得:X=8克
得:X=8克CH4+2O2
 CO2+2H2O
CO2+2H2O16 64
1克 Y
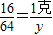 得:Y=4克
得:Y=4克2CO+O2
 2CO2
2CO256 32
1克 Z
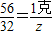 得:Z=0.57克
得:Z=0.57克通过计算、比较可知,相同质量的H2、CH4和CO,完全燃烧需要氧气的质量最多的是氢气,故A正确,B、C、D错误.
故选A.
点评:本题属于根据化学方程式的计算的无数据题,在计算时为了便于计算和比较,可假定质量都是1克,然后写出化学方程式并计算出氧气的质量,再进行比较即可.

练习册系列答案
相关题目
相同质量的H2、CH4和CO完全燃烧需要氧气的质量( )
| A、CO最多,H2最少 | B、H2最多,CH4最少 | C、H2最多,CO最少 | D、CH4最多,CO最少 |