题目内容
【题目】图示是用含SiO2杂质的BaCO3制备纳米碳酸钡的工艺流程,请回答下列问题:
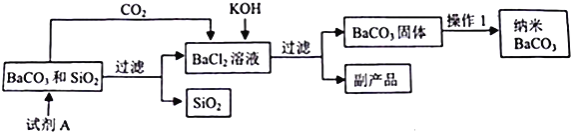
(1)试剂A的化学式是 .
(2)写出向BaCL2溶液加入KOH并通过CO2时发生的化学方程式
(3)操作1洗涤、检验和烘干,检验洗涤是否干净可选用试剂是
【答案】(1)HCl;(2)2KOH+CO2=K2CO3+H2O;K2CO3+BaCl2=BaCO3↓+2KCl;(3)AgNO3
【解析】(1)根据反应后生成氯化钡,由碳酸钡能与盐酸反应生成氯化钡、水、二氧化碳,可判断所加入的试剂A应为稀盐酸,溶质的化学式为HCl;故填:HCl;
(2)氢氧化钾和二氧化碳反应生成碳酸钾和水,碳酸钾和氯化钡发生反应生成碳酸钡沉淀和氯化钾,故填:2KOH+CO2=K2CO3+H2O;K2CO3+BaCl2=BaCO3↓+2KCl;
(3)为从反应后的混合溶液中获得纯净碳酸钡,需要进行过滤,过滤后洗涤沉淀表面残留的溶液,以除去沉淀表面可溶性杂质或残留滤渣表面滤液,然后进行烘干干燥;为检验洗涤干净,利用氯化钾能与硝酸银产生白色沉淀,可向洗涤后的溶液中滴加硝酸银检验洗涤后的溶液中不再含有氯化钾,以证明洗涤干净;故填:AgNO3.

【题目】某课外兴趣小组的同学设计了如下三个实验来验证质量守恒定律:

【设计并实验】
实验一:将盛有硫酸铜溶液的烧杯和铁钉一起放在托盘天平上称量,记录所称的质量.然后将铁钉浸到硫酸铜溶液中,观察现象.待反应一段时间后溶液颜色改变时,将盛有反应后物质的烧杯放在托盘天平上称量,记录所称的质量.
实验二:将盛有稀硫酸的烧杯和镁条一起放在托盘天平上称量,然后将镁条浸到稀硫酸中,观察现象.待反应一段时间后不再放出气泡时,将盛有反应后物质的烧杯放在托盘天平上称量,记录所称的质量.
实验一和实验二的数据见下表:
编号 | 实验一 | 实验二 |
反应前/g | 118.4 | 112.6 |
反应后/g | 118.4 | 112.4 |
实验三:用细线系住铜棒中点使之平衡,然后在铜棒一端用酒精灯加热.加热一段时间后,观察到铜棒的平衡情况是 .
【分析与讨论】
(1)在这三个实验中,你认为:实验 正确反映了反应物与生成物之间的质量关系,由此得出的结论是:在化学反应中生成物的总质量与反应物的总质量相等,请从原子的角度分析结论正确的理由是 .
(2)另外两个实验得出的结论是:在化学反应中生成物的总质量与反应物的总质量不相等,你认为导致这一结论错误的原因是 (只写其中一个实验的原因即可).
【实验反思】小组成员从不能正确反映反应物和生成物之间质量关系的两个实验中,找出了实验设计中的不当之处,并达成了以下共识:设计实验验证质量守恒定律时,对于有空气中的气体(成分)参与或有气体生成的化学反应,一般应使反应在 中进行.