题目内容
【题目】化学知识在生产,生活中有广泛的应用。
(1)生活中常用______方法降低水的硬度。
(2)日常生活中,切菜刀采用的防锈措施是_______。
(3)用下列物质除去油污时,利用乳化作用的是______(选填序号)。
A汽油 B洗洁精 C氢氧化钠溶液
(4)小苏打可用作治疗胃酸过多的药剂,用化学方程式表示其治疗原理_______。
(5)打开汽水瓶盖,有气泡冒出,说明气体溶解度随压强减小而______。
【答案】煮沸 保持刀表面清洁和干燥(或将刀表面洗净、擦干)(写涂油不给分) B NaHCO3+HCl=NaCl+H2O+CO2![]() 减小
减小
【解析】
(1)生活中常用煮沸的方法降低水的硬度,故填写:煮沸;
(2)切菜刀主要成分是铁,防止铁生锈采用避免接触水,即保持刀表面清洁和干燥,也可采用隔绝空气或氧气,日常生活中,常采用的防锈措施是:保持刀表面清洁和干燥,故填写:保持刀表面清洁和干燥(或将刀表面洗净、擦干);
(3)A、汽油能溶解油污,除去油污,不属于乳化,故不符合题意;
B、洗洁精可以乳化油污,从而除去油污,属于乳化,故符合题意;
C、氢氧化钠溶液能与油污反应,达到除去油污的目的,不属于乳化,故不符合题意;
(4)小苏打主要成分是碳酸氢钠,胃酸主要成分是稀盐酸,碳酸氢钠与稀盐酸反应生成氯化钠、水和二氧化碳,故填写:NaHCO3+HCl=NaCl+H2O+CO2![]() ;
;
(5)根据温度不变,气体的溶解度随压强的减小而减小的原理可知,打开汽水瓶盖,有气泡冒出,说明气体溶解度随压强减小而减小,故填写:减小。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案【题目】金属铁是当今用途最广的金属,现研究铁的冶炼。
(研究一)实验室模拟炼铁(装置如下图)。
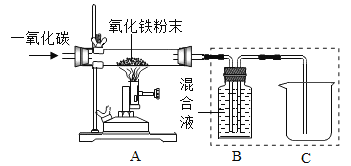
己知:B装置中的液体为过量的氢氧化钠与氢氧化钙混合液,氢氧化钠吸收二氧化碳能力比氢氧化钙强。请回答下列问题:
(1)实验过程中A处玻璃管中的实验现象:________。
(2)写出B处反应的化学方程式:________。
(3)实验装置按图连接,请将以下四步按正确操作步骤排序:________(填序号)。
A点燃A处酒精喷灯
B通入CO
C停止通入CO
D熄灭酒精喷灯
(4)实验装置图中虚线框内装置起到的作用有_________(填序号)。
A收集一氧化碳
B吸收二氧化碳
C检验二氧化碳
(5)己知此反应过程中温度不同,可能生成铁的不同的氧化物。原固体Fe2O3质量为48.0g,现用热分析仪记录CO与Fe2O3进行反应时有关数据,得到固体质量与反应温度的关系曲线如下图所示:
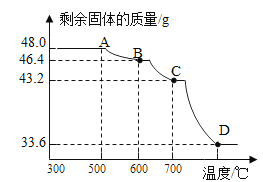
根据图象分析,写出B点时固体成分的化学式_________。
(研究二)工业炼铁(装置如下图)

(1)焦炭是炼铁的重要原料之一,其作用有___________。
(2)炼铁高炉内发生的主要化学反应①的化学方程式为____________。
(3)“高炉气体”中除二氧化碳外,体积含量最多的气体是___________。
(4)为测定产物生铁中单质铁的质量分数,某兴趣小组取用10g生铁样品,把100g稀硫酸分四次加入样品中(假设样品中除单质铁外,其他成份不与硫酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下:
稀硫酸的用量 | 剩余固体的质量 |
第一次加入25g | 7.2g |
第二次加入25g | 4.4g |
第三次加入25g | 1.6g |
第四次加入25g | 0.2g |
①从以上数据可知,第_________次生铁样品中的单质铁已完全反应。
②生铁样品中单质铁的质量分数=__________。
③所用稀硫酸的H2SO4质量分数。(列式计算)_______