题目内容
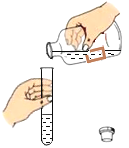
【题目】化学小组同学用下图所示装置(夹持仪器已略去)做了2个兴趣实验。每次实验时,打开止水夹,均可见C瓶内的水流入D中,B中有气泡逸出。
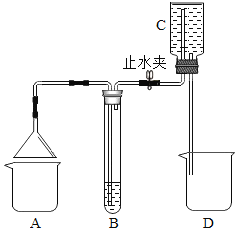
(1)在A处放燃烧的蜡烛,B中无色溶液变浑浊,B中的试剂是_____。蜡烛燃烧生成的气体被吸入B中的原因是_____。
(2)若A处放置浓盐酸,B中盛有紫色溶液甲,则变红色;若B中盛有红色溶液乙,则变无色。乙可能是_____。结合A、B两处物质的性质解释乙变色的原因:_____。
【答案】氢氧化钙溶液 C瓶内的水流入D中,使C瓶内压强小于大气压,A处气体被吸入B中 含有酚酞的碱性溶液 A中挥发出来的氯化氢气体进入B中,与B中碱性物质发生反应,使溶液红色褪去
【解析】
(1)A处的蜡烛燃烧后生成二氧化碳,二氧化碳能与无色的氢氧化钙溶液中的氢氧化钙反应生成碳酸钙沉淀使氢氧化钙溶液变浑浊,所以B中的试剂是氢氧化钙溶液,故填氢氧化钙溶液;
打开止水夹后, C瓶内的水流入D中,则C瓶中的压强减小且低于大气压,试管B中的压强随之减小,也小于大气压,所以A处蜡烛燃烧生成的气体被吸入B中,故填C瓶内的水流入D中,使C瓶内压强小于大气压,A处气体被吸入B中。
(2)如果乙是显碱性的物质与酚酞试液的混合物,当有酸性物质进入时,酸性物质能和减小物质发生化学反应,显碱性的物质逐渐消失,当减小物质完全消失后,溶液由红色变为无色,即乙是含有酚酞的碱性溶液,故填含有酚酞的碱性溶液;
A处的浓盐酸具有挥发性,挥发出来的氯化氢气体被吸入到B中,氯化氢进入B中溶于水形成盐酸,盐酸与B中的碱性物质反应生成盐和水使碱性物质消失,B中的酚酞由红色逐渐变为无色,故填A中挥发出来的氯化氢气体进入B中,与B中碱性物质发生反应,使溶液红色褪去。

 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案【题目】过氧化钠是化学中常见的一种药品,它是浅黄白色颗粒粉末.在空气中吸收水分和二氧化碳。易溶于水,与水中能发生反应生成氢氧化钠和过氧化氢,方程式:Na2O2+2H2O=2NaOH+H2O2,过氧化氢又能分解放出氧气。
(1)区分水和过氧化氢的实验方法是:___________________________,发生的反应方程式是:__________________________.
(2)某同学为了证明过氧化钠加入水中生成了氢氧化钠,在生成的溶液中滴加了几滴无色酚酞试液,观察到的现象是溶液先变红后褪为无色,请你对此现象进行探究.
提出问题:什么导致溶液先变红再褪色?
猜想与假设:
猜想1:甲同学“可能是无色酚酞溶液变质导致溶液褪色”;
猜想2:乙同学“可能是生成的过氧化氢使溶液褪色”.
实验与结论:
a:甲同学提出的猜想,立即遭到其他同学的反对,因为______________________________;
b:为了验证自己的猜想,乙同学设计了以下方案并实验验证:
实验步骤 | 实验现象 | 实验结论 |
取少量稀氢氧化钠溶液于试管中,滴加1﹣2滴酚酞试液,变红后,___________观察现象 | 溶液依然为红色 | ____________________ |
讨论交流:你还能提出不同的猜想吗?如果还能提出新的合理的假设和方案你将获得奖励分4分.
猜想3:_____________
方案3:
实验步骤 | 实验现象 | 实验结论 |
_________________ | _______________ | ______________ |