题目内容
【题目】将含有杂质的22克石灰石样品,放入盛有99.8克稀盐酸的烧杯中,石灰石中的碳酸钙与盐酸均恰好完全反应(杂质不参加反应),放出气体后,烧杯中剩余物质的质量为113克。请计算:
(1)生成二氧化碳的质量____________。
(2)反应后溶液中溶质的质量分数____________。
【答案】8.8g 20%
【解析】
(1)根据质量守恒定律可知,生成二氧化碳的质量=22g+99.8g-113g=8.8g;
(2)设生成8.8g二氧化碳需碳酸钙的质量为x,同时生成氯化钙的质量为y。
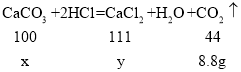
![]() x=20g;
x=20g;
![]() y=22.2 g;
y=22.2 g;
反应后溶液中溶质的质量分数=![]() 。
。
答:(1)生成二氧化碳的质量8.8g;
(2)反应后溶液中溶质的质量分数20%。

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
【题目】在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表.则关于此反应的说法正确的是( )
物 质 | X | Y | Z | W |
反应前的质量(g) | 2 | 1 | 16 | 16 |
反应后的质量(g) | 12 | m | 8 | 14 |
A.物质Y一定是该反应的催化剂
B.该反应的基本类型为分解反应
C.参加反应的Z与W的质量比为4:1
D.反应后生成X的质量为12 g