题目内容
【题目】(5分)氢化镁(MgH2)常被作为储氢介质,它与几种物质的转化关系如下。已知B、E之间发生中和反应,且F是一种盐酸盐。(所有的反应物和生成物均已标出)
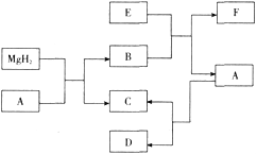
(1)写出E的化学式:____。
(2)在实验室发生A→C+D的反应条件是____。
(3)C作为一种新能源具有很多优点,试写出其中的一个优点:____。
(4)写出MgH2+A→B+C的化学方程式:____。
【答案】(1)HCl
(2)通电
(3)无污染(答案合理给分)
(4)MgH2+2H2O===Mg(OH)2+2H2↑
【解析】
试题分析:(1)B.E之间会发生中和反应,所以B.E是酸或碱中的一种,F盐酸盐,所以A是水,依据质量守恒定律可知,水和氢化镁反应生成氢氧化镁和氢气,所以B是氢氧化镁,C是氢气,那么E就是盐酸,A分解会生成氢气和D,所以D是氧气,氢化镁和水反应生成氢氧化镁和氢气,氢氧化镁和盐酸反应生成氯化镁和水,水在通电的条件下会生成氢气和氧气,推出的各种物质均满足题中的转化关系,推导合理,所以E是HCl;
(2)水在通电的条件下会生成氢气和氧气,所以A分解生成C.D的反应条件是:通电;
(3)氢气作为能源的燃烧产物是水,所以氢气具有的一个优点是:无污染(答案合理给分);
(4)氢化镁和水反应生成氢氧化镁和氢气,化学方程式为:MgH2+2H2O=Mg(OH)2+2H2↑.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案
相关题目