题目内容
【题目】向硝酸银、硝酸铜、硝酸镁的混合溶液中加入一些铁粉 ,待完全反应后 ,再过滤。下列情况不可能存在的是
A. 滤纸上有Ag ,滤液中有Ag+、Cu2+、Fe2+、Mg2+、
B. 滤纸上有Ag、Cu ,滤液中有Ag+、Fe2+、Mg2+
C. 滤纸有Ag、Cu ,滤液中有Cu2+ Fe2+ Mg2+
D. 滤纸上有Ag、Cu、Fe ,滤液中有![]()
【答案】B
【解析】
铁的金属活动性比银、铜强,比镁弱,向硝酸银、硝酸铜、硝酸镁的混合溶液中加入一些铁粉,铁不能与Mg(NO3)2溶液反应;铁先与AgNO3溶液反应生成硝酸亚铁溶液和银,AgNO3反应完,若还有贴粉,铁才能与Cu(NO3)2溶液反应生成硝酸亚铁溶液和铜,据此进行分析解答。
A、滤纸上有Ag,硝酸银溶液可能前恰好完全反应,也可能有剩余,则滤液中可能有Ag+、Cu2+、Fe2+、Mg2+,故选项说法正确;
B、滤纸上有Ag、Cu,说明硝酸银溶液已完全反应,则滤液中不可能含有银离子,故选项说法错误;
C、滤纸上有Ag、Cu,硝酸铜溶液可能前恰好完全反应,也可能有剩余,滤液中可能有Cu2+、Fe2+、Mg2+,故选项说法正确;
D、滤纸上有Ag、Cu、Fe,说明加入的铁是过量的,则滤液中有Fe2+、Mg2+,故选项说法正确。
故选B。

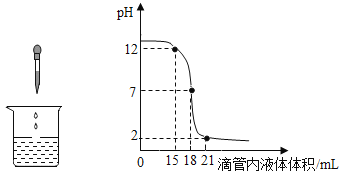
【题目】酸和碱能发生中和反应,它在日常生活和工农业生产中有着广泛的应用,如图表示稀盐酸和氢氧化钠溶液发生反应时烧杯中溶液的pH随加入液体体积的变化曲线及相关的实验操作,请从中获取信息,回答下列问题。
(1)①烧杯中盛放的是_____溶液。
②曲线上坐标为(15,12)的点所表示的意义:_____。
(2)小明完成上述实验几天后发现,忘记盖上盛放氢氧化钠溶液试剂瓶的瓶塞,请帮助小明完成如下实验方案来检验氢氧化钠溶液是否变质。
(提示:碳酸钠与氯化钡反应会生成碳酸钡沉淀和氯化钠)
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取少量溶液于试管中,滴加几滴稀盐酸 | _____ | 没有变质 |
方案二 | 取少量溶液于试管中,滴加几滴氯化钡溶液 | 产生白色沉淀 | 已经变质 |
你认为方案一的实验设计是否正确?请作出判断并说明理由:_____。
【题目】实验是科学探究的重要方法,让们一起再认识空气中氧气含量的测定拉瓦锡实验方案(如图1)利用汞的反应与图2相比,图2的优点_______(一条即可)
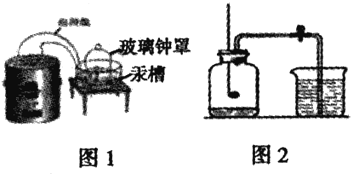
(实验回顾)兴趣小组的同学利用课本中的 实验方案(如图2)测定空气中氧气的含量,但测出的氧气的体积分数明显小于1/5。
请你参与探究:
(提出问题)造成误差的原因是什么?如何改进课本上的实验装置?
(查阅资料)红磷、白磷的一些性质如下表:
颜色、状态 | 熔点/℃ | 着火点/℃ | 密度/(g/cm3) | |
红磷 | 暗红色固体 | 590 | 240 | 2.34 |
白磷 | 白色或黄色固体 | 44.1 | 40 | 1.82 |
(猜想与假设)
甲同学;可能是导管内原含有空气,后来残留有吸入的水,影响实验的准确性。
乙同学:可能是瓶内残留气体中还有氧气。
你还能作出的猜想是____________。
(实验与交流)在老师的指导下,小组同学对课本上的实验装置进行了图3所示的改进(其他仪器忽略)。
(1)甲同学提出应把红磷换为白磷,理由是________________________。
(2)写出白磷燃烧的化学方程式________________________。
(3)与课本上的实验装置相比较,该装置的一个优点是________________________。
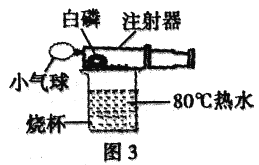
(探究与反思)
(4)大家用改进的实验装置进行实验,待注射器冷却、管内白烟消失后,又意外发现注射器内壁附着黄色固体,该黄色固体的主要成分可能是______________________。
(5)为了验证乙同学的猜想,在老师的指导下,兴趣小组 的闻学又利用传感器改进实验装置(如图4),分别用过量的红磷和白磷进行对照实验,并用高能激光笔点燃磷。
①用测量氧气浓度的传感器测得反应后装置内氧气 浓度分别是:红磷为8.7%和白磷为1.0% ,从而证明乙同学的猜想___________(填“正确”或“错误”),但也有同学认为白磷也不能准确测定空气中氧气含量的原因是_________________________________。
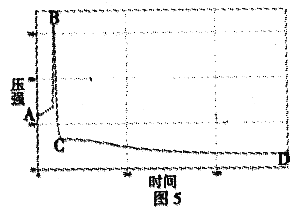
②如图5是白磷燃烧过程中的压强变化趋势,试分析回答:图中AB段变化的原因是______________________; BC段变化的原因是______________________。