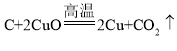题目内容
【题目】某兴趣小组为探究金属活动性强弱,分别做了镁、铝、铜与稀盐酸反应的实验。
(1)比较金属活动性强弱:铝比铜________(填“强”或“弱”),比较的依据:_________。写出镁与稀盐酸反应的化学方程式:_____________。
(2)小芳同学做镁与稀盐酸反应的实验时,发现试管中出现灰白色沉淀,该小组同学对灰白色沉淀的成分进行如下探究:
(提出假设)
假设一:含有氯化镁
假设二:含有镁粉
假设三:含有氢氧化镁 ……
(查阅资料)①氯化镁易溶于水;②在一定条件下,镁可与冷水缓慢反应。
(设计并进行实验)各取少量灰白色沉淀加入两支试管中,进行如下实验:
编号 | 实验操作 | 实验现象 |
实验1 | 加入适量蒸馏水,搅拌 | 沉淀未见减少 |
实验2 | 加入适量稀盐酸 | 沉淀全部溶解,没有气泡产生 |
(得出结论)由实验1可知,假设__________不成立;由实验2可知,沉淀中不含_______。
假设三_____________(填“成立”、“可能成立”或“不成立”)。
(实验反思)实验后同学们请教老师得知,灰白色沉淀的主要成分是碱式氯化镁,碱式氯化镁受热易分解产生氯化氢气体。于是小芳再取少量灰白色沉淀于试管中加热,并将蘸有紫色石蕊溶液的滤纸条悬于试管口,预期的实验现象是_____________。
【答案】强 铝可以和盐酸反应,铜不和盐酸反应 ![]() 一 镁粉 可能成立 滤纸条变红
一 镁粉 可能成立 滤纸条变红
【解析】
(1)比较金属活动性强弱:铝比铜强,比较的依据是:铝可以和稀盐酸反应,有气泡产生,铜不和稀盐酸反应,无现象,说明在金属活动性顺序里,铝位于氢之前,铜位于氢之后,铝的金属活动性比铜强;
镁与稀盐酸反应生成氯化镁和氢气,其化学反应方程式是:![]() ;
;
(2)得出结论:加适量蒸馏水、搅拌,沉淀未见减少,说明沉淀中无氯化镁,因为氯化镁易溶于水,假设一不成立,实验2:加入适量稀盐酸,沉淀全部溶解,没有气泡产生,因为镁能和稀盐酸反应生成氢气,由实验2可知,沉淀中不含镁粉,沉淀全部溶解,氢氧化镁可以和稀盐酸反应生成氯化镁和水,氯化镁易溶于水,故假设三可能成立;
实验反思:碱式氯化镁受热易分解产生氯化氢气体,氯化氢气体溶于水生成盐酸,盐酸呈酸性,可使紫色石蕊溶液变红,故预期的实验现象是滤纸条变红。

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】为确定某大理石样品的纯度,某兴趣小组进行如下实验:称取该大理石(主要成分是CaCO3,杂质不参加反应)加入烧杯中,向其中逐渐加入稀盐酸至完全反应。反应结束后,称量烧杯及其中物质的总质量(溶解的气体忽略不计),有关数据记录如下表。
烧杯 | 大理石 | 稀盐酸 | 反应后烧杯及其中物质总质量 | |
质量/g | 90 | 8.5 | 50 | 145.2 |
(1)实验中判断碳酸钙已经完全反应的方法是_____。
(2)实验中产生的二氧化碳质量为_____克。
(3)请计算该大理石样品的纯度_____。(计算结果精确到0.1%)。
【题目】下列有关叙述、对应的化学方程式、所属基本反应类型一一对应且都正确的是( )
选项 | 叙述和化学方程式 | 基本反应类型 |
A | 拉瓦锡测得空气中氧气含量: | 分解反应 |
B | 酸雨的形成: | 化合反应 |
C | 实验室用锌和稀硫酸反应制氢气: | 置换反应 |
D | 碳与灼热的氧化铜反应: | 还原反应 |
A.AB.BC.CD.D
【题目】张玲同学为测定汉白玉中碳酸钙的质量分数,称取5.55g研碎的汉白玉粉末进行四次高温加热、冷却、称量剩余固体的重复操作。记录数据如下:
操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量(g) | 4.25 | 3.95 | 3.35 | 3.35 |
请计算:
(1)完全反应后产生的二氧化碳质量_____;
(2)汉白玉中碳酸钙的质量分数________。