题目内容
【题目】如图是提纯CO、CO2混合气体中的CO并还原氧化铁的示意图.请回答有关问题:
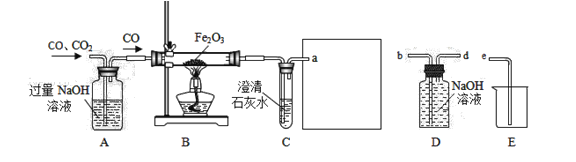
(1)为避免一氧化碳污染空气,并回收利用一氧化碳,方框中连接的是D和E,导管接口的连接顺序为a→_____→_____→e.D装置中NaOH的作用是_______________.如果导管连接错误,后果是____________________.
(2)实验进行一段时间后,B装置的玻璃管中的现象为_________________,反应方程式为______________________.
(3)取实验后D中的混合溶液,利用实验室的试剂和条件,制取氢氧化钠固体。实验步骤如下(其中Ⅰ、Ⅱ、Ⅲ为实验操作):
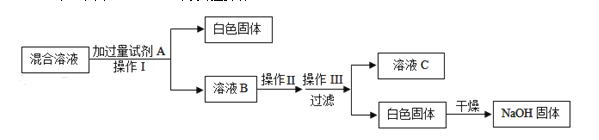
①试剂A是微溶于水的碱,其化学式为______________;
②操作Ⅱ的为名称为蒸发浓缩,操作Ⅲ的为名称为_______________.
③如果在操作Ⅱ的过程中,溶液B中出现少量浑浊,原因可能是__________________.
【答案】d b 吸收C装置中没反应掉的二氧化碳 会造成CO排入空气中会污染空气 红棕色固体变黑 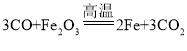
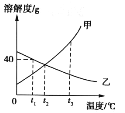
![]() 过滤 氢氧化钙的溶解度随温度的升高而减小,温度升高,有氢氧化钙析出
过滤 氢氧化钙的溶解度随温度的升高而减小,温度升高,有氢氧化钙析出
【解析】
二氧化碳和氢氧化钠反应生成碳酸钠和水,氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳。
(1)一氧化碳有毒,不能排放到空气中去,一氧化碳密度比空气小,一氧化碳收集,导管要短进长出,故导管接口的连接顺序为d、b、e,排出的氢氧化钠溶液流到E中的烧杯中去,二氧化碳和氢氧化钠反应生成碳酸钠和水,故D装置中NaOH的作用是吸收C中没反应掉的二氧化碳;如果导管连接错误,会造成CO排入空气中会污染空气。
(2)氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳,氧化铁是红棕色粉末,所以会看到红棕色固体变黑,反应的化学方程式是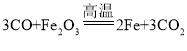 。
。
(3)①试剂A是微溶于水的碱,混合溶液和A生成白色固体和溶液B,故A是氢氧化钙,化学式为![]() 。
。
②操作Ⅱ的为名称为蒸发浓缩,操作Ⅲ的为名称为过滤。
③如果在操作Ⅱ的过程中,溶液B中出现少量浑浊,原因可能是氢氧化钙的溶解度随温度的升高而减小,温度升高,有氢氧化钙析出。

【题目】煅烧石灰石(主要成分 CaCO3)生成生石灰(CaO)和二氧化碳。为了测定某石灰石中碳酸钙(CaCO3)的含量,现称取 24.0g 石灰石样品,进行四次高温煅烧、冷却,称量剩余固体的质量 (杂质不参加反应),记录实验数据如下:
操作 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量 | 21.6g | 19.2g | 15.2g | 15.2g |
试计算:
(1)完全反应后生成二氧化碳的质量为_____;
(2)求该石灰石样品中碳酸钙的质量_____。
【题目】在一密闭容器中放入X、Y、M、N四种物质,在一定条件下发生化学反应,一段时间后,测得有关的数据如下,则关于此反应认识正确的是( )
物质 | X | Y | M | N |
反应前质量(g) | 16 | 2 | 35 | 5 |
反应后质量(g) | 3 | 17 | 13 | 待测 |
A.该反应一定是置换反应B.反应中X和Y的质量比为8:1
C.反应后N的质量为25D.该反应X和Y都是反应物