��Ŀ����
����Ŀ���ó涣ҧʱ����������ᡣ��ѧС��ͬѧ�����������Ũ���ͷȤ�������������̽����
[�������]����ijɷ���ʲô?.����ʲô���ʣ�
[��������]
������Ļ�ѧ���ƽм��ᣬ��ѧʽΪHCOOH
�������������������ʱ��ֽ���������������
��Ũ���������ˮ��
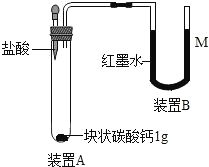
[ʵ��̽��]��1����ʢ��������Һ���Թ��еμ���ɫʯ����Һ���۲쵽��Һ��ɫ��ɺ�ɫ,˵�����������ԡ�
��2��С��ͬѧ���������к���_________Ԫ��, �Ʋ�������ڸ������������ȷֽ�ʱ����ˮ��
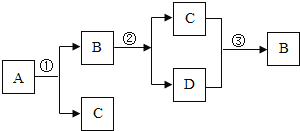
��3�������ֽ����ɵ���һ�������С��������ֲ��룺
����I��CO2������II�ǣ�_______________��
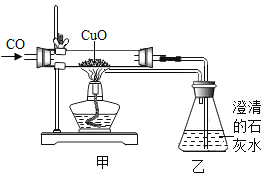
���ǰ���ͼ��ʾ����ʵ�飺����A��ͨ��һ���N2�ٽ�����ֽ����������ͨ�����С�
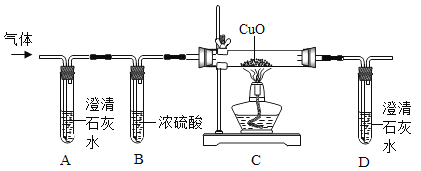
����ͨN2��Ŀ����______________��
����װ��A�������Ա仯�������I_____________��(����������������������);
��װ��B��������______________��
��ʵ��ʱװ��C�е�������_____________��
��װ��D�еĻ�ѧ��Ӧ����ʽ��____________��
[����]�����������������ʱ�Ļ�ѧ����ʽ_______________��
[���۽���]�ӻ����Ƕȿ�����װ�ô��ڵ�����ȱ����_______������������______________��
���𰸡��� CO �ų�װ���еĿ��� ������ ��ȥ�����е�ˮ���� �����ɺ�ɫ��ɺ�ɫ CO2+Ca��OH��2�TCaCO3��+H2O HCOOH![]() H2O+CO�� ȱ��β������ ��β����һ��ȼ�ŵľƾ���
H2O+CO�� ȱ��β������ ��β����һ��ȼ�ŵľƾ���
��������
[ʵ��̽��] ��2��С��ͬѧ���������к�����Ԫ�أ��Ʋ�������ڸ������������ȷֽ�ʱ����ˮ��
��3�������к���̼Ԫ�أ�̼Ԫ�ص���������һ����̼�Ͷ�����̼�����ֽ����ɵ���һ�������С��������ֲ��룺�������CO2���������CO��
����ͨN2��Ŀ�����ų�װ���еĿ�������ֹӰ��ʵ������
����װ��A�������Ա仯��˵�������в����ж�����̼������������
��Ũ���������ˮ�ԣ�װ��B�������dz�ȥ�����е�ˮ������
��һ����̼������ͭ��Ӧ������ͭ�Ͷ�����̼��װ��C�е������ǹ����ɺ�ɫ��ɺ�ɫ��
��ʵ��ʱװ��D�з�����Ӧ�Ƕ�����̼���������Ʒ����˷�Ӧ����Ӧ�Ļ�ѧ����ʽΪ��CO2+Ca��OH��2�TCaCO3��+H2O��
[����] �������ȷֽ�Ϊˮ��һ����̼����Ӧ�Ļ�ѧ����ʽΪHCOOH![]() H2O+CO����
H2O+CO����
[���۽���] ����һ����̼�ж�����Ⱦ�������ӻ����Ƕȿ�����װ�ô������Ե�ȱ����ȱ��β�����������������ǣ���β����һ��ȼ�ŵľƾ��ơ�

 ��ְٷְټ���ϵ�д�
��ְٷְټ���ϵ�д� �����ƻ���ĩ��̶�100��ϵ�д�
�����ƻ���ĩ��̶�100��ϵ�д�