题目内容
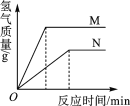
【题目】相同质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如图所示。下列有关叙述正确的是( )
A. 金属活动性:N>M
B. 生成H2的质量相等
C. 相对原子质量:M>N
D. 消耗盐酸的质量不相等
【答案】D
【解析】
A、根据图像可以看出,纵坐标表示氢气质量,横坐标表示反应时间,斜率表示反应的速度,M的斜率比N的大,所以M比N反应的速度快,所以金属活动性: M>N,故A错误;
B、根据图像可知,M产生的氢气多,N产生的氢气少,两种金属产生的氢气质量不同,故B错误;
C、根据图像可知,M产生的氢气比N多,M、N在生成物中均为+2价,价态相同的金属与足量的酸反应,相对原子质量越大,产生的氢气越少,说明N的相对原子质量大,故C错误;
D、若两个反应消耗盐酸的质量,则置换出的氢的质量相等,产生的氢气的质量应该相同,而由图像可以看出,产生的氢气质量不相等,所以消耗盐酸的质量不相等,故D正确。故选D。

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
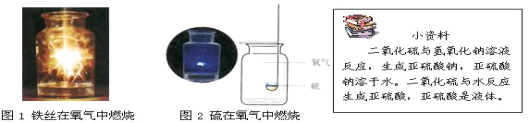
【题目】某同学利用“多米诺骨牌”效应,设计了如图气体制取与性质验证的组合实验,打开A中分液漏斗的活塞,很快看到E中导管口有气泡冒出,且溶液由紫色变红色。 请看图回答问题:
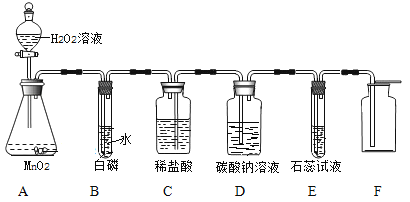
(1)A中反应的化学方程式 ;
B中白磷不燃烧,原因是 。
(2)C、D中看到的现象分别是 、
。
(3)用化学方程式表示E中颜色变化的原因 。
(4)将D中液体倒入试管中,对其成分进行探究:
实验操作 | 实验现象 | 结论 |
方法一:向试管中滴入 溶液 | 无色液体变白色浑浊 | 溶质中一定含有 碳酸钠和 |
方法二:向试管中放入镁条 | 气泡产生 |