��Ŀ����
����Ŀ���������ճ������г��õ������Ʒ�����ź��ƾõ���ʷ.����̼��ƿ���������Ħ��������ҵ�ϳ���ʯ��ʯ�������������ʣ����Ʊ��Ƚϴ���������̼��ơ�
��֪����ʯ��ʯ�������տ���������ʯ�ҺͶ�����̼���������������Ӧ������ʣ�ࡣ
����ʯ����ˮ��ַ�Ӧ��ɵõ������dz�ϸС����ʯ�ҽ���
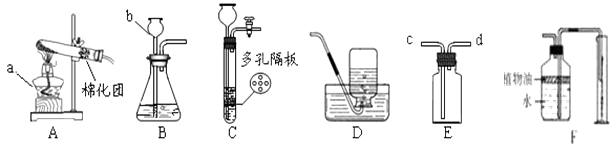
ijʵ��С��ͬѧ�����2��ת�����̣�����ͼ��ʾ��
��ش��������⣺
��1����������ʯ��ʯ��Ӧ�Ļ�ѧ����ʽ�� �� �÷�Ӧ��������Ӧ��
��2������������������IJ����������ձ����������� �� ����������������
��3�����÷�Ӧ�٢ڢ��Ʊ�����̼��Ƶķ����ŵ��У�д��һ�ּ��ɣ���
��4�����÷�Ӧ�٢ڢ��Ʊ�����̼��Ƶķ����ŵ��У�д��һ�ּ��ɣ���
���𰸡�
��1��CaCO3 ![]() CaO +CO2�����ֽⷴӦ
CaO +CO2�����ֽⷴӦ
��2��©������������
��3������Ҫ�������ӷ�Ӧ���Լ�ɱ�
��4����Һ֮��ķ�Ӧ�����У�����ͬʱ������Ҫ�Ĺ�ҵԭ�ϡ����������Ƶ�
���������⣺��1��ʯ��ʯ���ջ������������������̼��CaCO3 ![]() CaO+CO2�����÷�Ӧ�����ǷֽⷴӦ�� ��2������������������IJ����������ձ�����������©�������������������������ã���3���٢ڢ�ʹ�õ��������������ɵĶ�����̼���ȿ��Բ���Ҫ�������ӷ�Ӧ���Լ�ɱ���Ҳ�ܼ�������ЧӦ����4���٢ڢ�������Һ֮��ķ�Ӧ�����У�ͬʱ��������������һ����Ҫ�Ļ���ԭ�ϡ���һ�������ڽ���ʱҪ���������ͼ�е�ÿһ�����裬�˽�ÿһ�������н��������ʣ�������ʲô��Ӧ���ò�������Ŀ����ʲô����������ᴿ��Ʒ����ʲô�������õȡ���Ҫ�ж����ӵ��Լ������ԴӼ����Լ���Ŀ�ġ���Ӧ�IJ������ֽ��з�������Ҫ�ж�����ͼ��ijһ���е����ʿ��Դ���һ�������з�Ӧ����ܷ����ķ�Ӧ���ֽ��з�����ͬʱ��ע�������Լ��Ƿ���ʣ�ࡣ�۸�������ͼ��д����ij���з�����Ӧ�Ļ�ѧ����ʽ������Ҫ�ҳ�����ò������е����ʣ�������ѧ֪ʶ�ж�����ܷ����ķ�Ӧ��Ȼ��д�������������ƽ��
CaO+CO2�����÷�Ӧ�����ǷֽⷴӦ�� ��2������������������IJ����������ձ�����������©�������������������������ã���3���٢ڢ�ʹ�õ��������������ɵĶ�����̼���ȿ��Բ���Ҫ�������ӷ�Ӧ���Լ�ɱ���Ҳ�ܼ�������ЧӦ����4���٢ڢ�������Һ֮��ķ�Ӧ�����У�ͬʱ��������������һ����Ҫ�Ļ���ԭ�ϡ���һ�������ڽ���ʱҪ���������ͼ�е�ÿһ�����裬�˽�ÿһ�������н��������ʣ�������ʲô��Ӧ���ò�������Ŀ����ʲô����������ᴿ��Ʒ����ʲô�������õȡ���Ҫ�ж����ӵ��Լ������ԴӼ����Լ���Ŀ�ġ���Ӧ�IJ������ֽ��з�������Ҫ�ж�����ͼ��ijһ���е����ʿ��Դ���һ�������з�Ӧ����ܷ����ķ�Ӧ���ֽ��з�����ͬʱ��ע�������Լ��Ƿ���ʣ�ࡣ�۸�������ͼ��д����ij���з�����Ӧ�Ļ�ѧ����ʽ������Ҫ�ҳ�����ò������е����ʣ�������ѧ֪ʶ�ж�����ܷ����ķ�Ӧ��Ȼ��д�������������ƽ��