题目内容
【题目】人类的日常生活和工农业生产离不开水。请回答:
(1)水__________(填“属于”或“不属于”)人类所需的六大基本营养素之一。
(2)含有较多可溶性钙、镁化合物的水叫做__________(填“软水”或“硬水”)。
(3)自来水净化中用来消毒用的氯气是一种黄绿气的气体,如果出现氯气泄露,可用烧碱溶液来吸收处理,其化学反应原理为:Cl2+2NaOH=X+NaClO+H2O,则X的化学式是__________。
(4)下图为某同学进行电解水实验的装置图,C试管中收集到的气体是__________,在水的电解实验中,没有发生改变的微粒是__________。

(5)电解水时常加入氢氧化钠增强导电性,现有5%的氢氧化钠溶液100g,通电一段时间后,测得氢氧化钠溶液的浓度变为10%.反应中被电解水的质量是__________g。
(6)水是实验室最常见的溶剂。用浓硫硫酸配制稀硫酸时,用到的玻璃仪器有烧杯、量筒、玻璃棒和__________。
【答案】 属于 硬水 NaCl O2 氢原子种类和氧原子种类 50 胶头滴管
【解析】(1)水属于人类所需的六大基本营养素之一;
(2)含有较多可溶性钙、镁化合物的水叫做硬水;
(3)由Cl2+2NaOH═X+NaClO+H2O可知,反应前后氧原子都是2个,氢原子都是2个,反应前氯原子是2个,反应后应该是2个,其中1个包含在X中,反应前钠原子是2个,反应后应该是2个,其中1个包含在X中,则X的化学式是NaCl;
(4)C试管中收集到的气体是氧气,在水的电解实验中,没有发生改变的微粒是氢原子和氧原子;
(5)设电解水的质量为x,
根据题意有: ![]() =10%,
=10%,
x=50g;
(6)水是实验室最常见的溶剂,用浓硫酸配制稀硫酸时,用到的玻璃仪器有烧杯、量筒、玻璃棒和胶头滴管。

【题目】某钙片的标签如图,且知此钙片成分中只有碳酸钙含有钙元素。
主要成分:碳酸钙(CaCO3)维生素D |
规 格:每瓶50片,净重40克 |
含 钙 量:每片含钙0.75克 |
(1)其中维生素D2有助于钙的吸收,它的化学式为C28H44O,它的相对分子质量为_______;
(2)根据标签中的含钙量计算出,每片该片中碳酸钙的含量为_________g;
(3)标签中的含钙量是否合理__________(填“是”或“否”)?
【题目】实验课上,某小组的同学用生石灰进行“化学反应中能量的变化”实验时发现:向块状生石灰中加入适量水后没有明显的温度变化。为确定其原因,进行了如下实验探究。
【提出问题】生石灰是否变质?其成分是什么?
【查阅资料】氢氧化钙溶解过程中无明显温度变化,与盐酸反应无气体生成。
【猜想与假设】同学们认为生石灰样品已经变质,并对其成分作出了如下4种猜想。
猜想1:氧化钙和氢氧化钙;
猜想2:氧化钙和碳酸钙;
猜想3:______;
猜想4:氧化钙、氢氧化钙和碳酸钙。
【进行实验】同学们将少量样品研碎后,按如图所示过程进行实验。
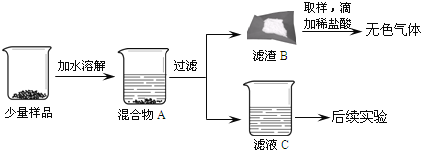
(1)在溶解过程中用温度计测量液体的温度,发现温度计示数升高,说明样品中应该含有____________。结论:猜想3不成立。
(2)滤渣B中一定含有________,用化学方程式表示生成该物质的反应________。
结论:①块状生石灰表面发生变质;②猜想1不成立。
(3)为验证滤液C的成分,进行后续实验。
实验操作 | 实验现象 | 实验结论 |
______ | ______ | ①滤液中溶质为氢氧化钙 ②猜想4成立,猜想2不成立 |
【反思与评价】
有的同学认为上述实验过程不能得出猜想4成立、猜想2不成立的结论,理由是_________。



