题目内容
【题目】(4分)下表是元素周期表中的1~18号元素原子核外电子排布,我们对它进行研究:
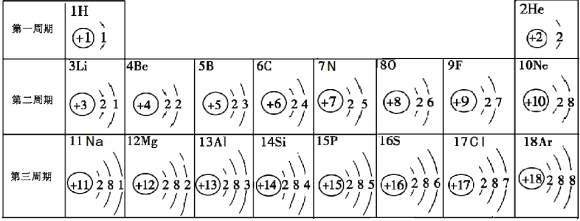
(1)写出硫元素的一种氧化物的化学式 。
(2)写出质子数为1、6、8、11四种元素组成的可以治疗胃酸过多物质的化学式: 。
(3)![]() 表示一种元素的两种粒子,它们属于同一种元素的依据是 。
表示一种元素的两种粒子,它们属于同一种元素的依据是 。
(4)图中He与Ne、Ar原子最外层电子数不一样,但都处在每周期的结尾处,从原子结构上分析其原因 。
【答案】(1)SO2或SO3 (2)NaHCO3 (3)这两种微粒的质子数相同
(4)氦原子只有一个电子层,只能容纳2个电子,与Ne、Ar原子一样,它们的最外层电子数都达到稳定结构
【解析】
试题分析:(1)硫元素的常见化合价为+4、+6,所以一种氧化物的化学式:SO2或SO3
(2)质子数为1、6、8、11四种元素分别是氢、碳、氧、钠,组成的可以治疗胃酸过多物质的化学式:NaHCO3
(3)决定元素种类的是质子数,所以它们属于同一种元素的依据是:这两种微粒的质子数相同
(4)图中He与Ne、Ar原子最外层电子数不一样,但都处在每周期的结尾处,是因为:)氦原子只有一个电子层,只能容纳2个电子,与Ne、Ar原子一样,它们的最外层电子数都达到稳定结构

 阅读快车系列答案
阅读快车系列答案【题目】(5分)某实验小组利用废硫酸液制备K2SO4的流程如下:
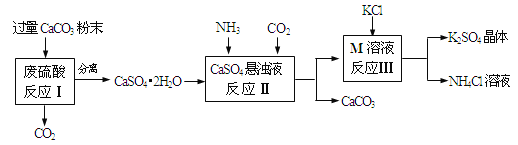
⑴ 将CaCO3研成粉末的目的是 。
⑵ 上述流程中可循环使用的物质有CO2和 (填写化学式)。
⑶ 反应Ⅲ中相关物质的溶解度如下表所示。你认为反应Ⅲ在常温下能实现的原因是
。
物质 | KCl | K2SO4 | NH4Cl | M |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
⑷ 为了得到较纯的K2SO4晶体,常用饱和K2SO4溶液洗涤反应Ⅲ所得晶体。为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入 (选填序号,下同),振荡、静置,再向上层清液中滴加 ,观察现象即可判断。
a.AgNO3溶液 b.过量的BaCl2溶液 c.过量的Ba(NO3)2溶液
【题目】(5分)在宏观、微观和符号之间建立联系是学习化学的基本方法。
(1)下列为A、B、C、D的原子或离子的结构示意图。
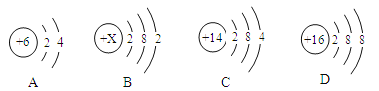
①B的原子结构示意图中X为 ;若D的元素符号为S,则D表示的微粒符号是 。
②分析A、C的原子结构,你认为A与C具有相似化学性质的原因是 。
(2)下图为处理汽车尾气化学反应微观示意图,其中A、B、C、D表示4种物质,A和B在一定条件下反应可生成C 和D。
反应前 | 反应后 |
| ||
|
|
|
| |
③物质C中,各元素的质量比为 。
④根据上述微观示意图,处理汽车尾气的化学反应方程式为 。



